Titan (IV) -Chlorid – Wikipedia
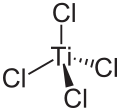
| Formule structurelle | |
|---|---|
 |
|
| Général | |
| Nom | Titan (iv) – Chloride |
| Autres noms |
Titantetrachloride |
| Formule de purée | Ticl 4 |
| Brève description |
Incolore, piquant odeur, liquide fortement fumé sur l’air humide [d’abord] |
| Identificateurs / bases de données externes | |
| Caractéristiques | |
| Masses molaires | 189,71 g · mol −1 |
| État global |
fluide |
| densité |
1 728 g · cm −3 [2] |
| Point de fusion |
−24,1 ° C [2] |
| point d’ébullition |
136,4 ° C [2] |
| La pression de la vapeur |
|
| solubilité | |
| Indice de réfraction |
1 6076 (18 ° C) [3] |
| consignes de sécurité | |
| Dans la mesure du possible et commun, des unités SI sont utilisées. Sauf indication contraire, les données fournies s’appliquent aux conditions standard. Index de réfraction: ligne Na-D, 20 ° C | |
Titan (iv) – Chloride ( Titantetrachloride ) est un composé chimique du chlore et du titane. Le titane est en ticl 4 dans son niveau d’oxydation le plus élevé et le plus stable.
D’autres composés de chlore du titane, y compris le chlorure de titan (III), qui est un agent de réduction fort, sont connus. [5]
Le titantetrachlorure est fabriqué par glucide de dioxyde de titane en présence de charbon et de chlore à 700–1000 ° C: [d’abord]
- [6] La fonction de pression de vapeur se traduit en conséquence Antoine dix (P) = a – (b / (t + c)) (p dans tor, t en ° C) avec a = 6,79094, b = 1348,56 et c = 208,52 dans la plage de température de 40 à 142 ° C. [6] Titantetrachlorure hydrolysé avec de l’eau dans une réaction exothermique violente au dioxyde de titane et au chlore d’hydrogène. Cependant, il n’y a pas de dioxyde de titane pur, mais un chlore d’eau et d’hydrogène. [7] [8]
- [8] L’hydrolyse a déjà lieu lorsque vous contactez l’humidité de l’air, avec des vapeurs blanches en chlore d’hydrogène sur le tissu. [7]
Le titantetrachlorure est un acide Lewsic important et est en chimie organique dans les réactions de Knoevenagel
et la réaction Mukaiyama Michael utilisée. Il s’agit également du matériau de base pour les catalyseurs, tels que les catalyseurs Ziegler-Natta, et le matériau de départ pour les composés organo-titanium.
Le titantetrachlorure est utilisé dans les producteurs de tabagisme à des fins militaires (FOG Fighting Substance). Le titantetrachlorure se produit comme un intermédiaire lors du nettoyage du dioxyde de titane (“procédure de chlorure”) et de la production de titane (“procédé Kroll”). Il est également utilisé dans la chimie analytique humide pour détecter les peroxydes. En cas d’estimation du peroxyde, la solution devient jaunâtre en orange.Surtout dans l’utilisation militaire comme matériau de lutte contre le brouillard, il existe un risque d’inhaler le chlore d’hydrogène résultant. Cela peut être aussi
Des brûlures supplémentaires ou même des muqueuses ou du tissu pulmonaire.
Les premiers symptômes lors de l’inhalation sont la toux et les douleurs thoraciques. Si les symptômes durent plus de 20 minutes, un œdème pulmonaire menaçant la vie peut être attendu, ce qui peut se produire même sans symptômes persistants.- ↑ un b c d Saisir Titanchlorure . Dans: Römppp en ligne. Georg Thieme Verlag, consulté le 29 septembre 2014.
- ↑ un b c d C’est F g H je Saisir Titan (iv) – Chloride Dans la base de données Gestis Tabric de l’IFA, consultée le 9 décembre 2019. (JavaScript requis)
- ↑ David R. Lide (éd.): CRC Handbook of Chemistry and Physics . 90. AUFLAGE. (Version Internet: 2010), CRC Press / Taylor et Francis, Boca Raton FL, Indice de réfraction des liquides inorganiques , S. 4-140.
- ↑ Saisir Tétrachlorure de titane dans le Inventaire de classification et d’étiquetage L’Agence européenne chimique (ECHA), consultée le 1er février 2016. Le fabricant ou le charme traditionnel peut être la classification et l’étiquetage harmonisés développer .
- ↑ Pour déterminer le loriure de titane et le trichlorure dans la fonte alcaline alcaline ou terrestre , dans Journal de la chimie analytique de Fresenius , 171/1959, S. 151–152
- ↑ un b Pike, F.P.; Foster, C.T.: Pression de vapeur et point d’ébullition du tétrachlorure de titane Dans J. Chem. Eng. Données 4 (1959) 305–306.
- ↑ un b Kapias, T.; Griffiths, R.F.: Sormes accidentelles de tétrachlorure de titane (TICL 4 ) Dans le contexte des principaux dangers – un comportement de transfert en utilisant Reactpool Dans J. Hazard. Mater. 119 (2005) 41–52, doi: 10.1016 / j.jhazmat.2004.12.001 .
- ↑ un b Vechot, L.; Buston, J.E.H.; Kay, J.; Round, G.A.; Masharani, S.; Tickle, G.A.; Rowlands, r .: Étude expérimentale de la réaction d’hydrolyse en phase liquide du tétrachlorure de titane . Dans: I. Chem. E. Symp. Série 156 (2011) 238-245.
- [8] L’hydrolyse a déjà lieu lorsque vous contactez l’humidité de l’air, avec des vapeurs blanches en chlore d’hydrogène sur le tissu. [7]
 [6] La fonction de pression de vapeur se traduit en conséquence Antoine dix (P) = a – (b / (t + c)) (p dans tor, t en ° C) avec a = 6,79094, b = 1348,56 et c = 208,52 dans la plage de température de 40 à 142 ° C. [6] Titantetrachlorure hydrolysé avec de l’eau dans une réaction exothermique violente au dioxyde de titane et au chlore d’hydrogène. Cependant, il n’y a pas de dioxyde de titane pur, mais un chlore d’eau et d’hydrogène. [7] [8]
[6] La fonction de pression de vapeur se traduit en conséquence Antoine dix (P) = a – (b / (t + c)) (p dans tor, t en ° C) avec a = 6,79094, b = 1348,56 et c = 208,52 dans la plage de température de 40 à 142 ° C. [6] Titantetrachlorure hydrolysé avec de l’eau dans une réaction exothermique violente au dioxyde de titane et au chlore d’hydrogène. Cependant, il n’y a pas de dioxyde de titane pur, mais un chlore d’eau et d’hydrogène. [7] [8]
![{displaystyle {ce {TiCl4 + 3H2O -> [TiO2*H2O*3HCl] + HCl}}}”></span></dd>
</dl>
<p>La chaleur d’hydrolyse est de -295 kJ · mol <sup>−1 </sup>. <sup id=](https://wikimedia.org/api/rest_v1/media/math/render/svg/4eec8490bbcf2ddb39dbad721730bc66a7518350) [8] L’hydrolyse a déjà lieu lorsque vous contactez l’humidité de l’air, avec des vapeurs blanches en chlore d’hydrogène sur le tissu. [7]
[8] L’hydrolyse a déjà lieu lorsque vous contactez l’humidité de l’air, avec des vapeurs blanches en chlore d’hydrogène sur le tissu. [7]
Recent Comments