Balance du liquide de vapeur-wikipedia

Le Équilibre de liquide de vapeur (Surtout comme Vouloir Décrit après l’anglais Équilibre de vapour-liquide ) est un équilibre de phase dans lequel il y a un liquide et une vapeur ou un gaz dans l’équilibre thermodynamique. L’équilibre à vapeur-fluide est également caractérisé par le fait que la quantité de tissu qui évapore la quantité de tissu y correspond. Le potentiel chimique est également le même dans les deux phases.
Un équilibre de liquide de vapeur est clairement déterminé dans les substances pures par la pression et la température des tailles, avec des mélanges, les compositions de la phase liquide et en forme de vapeur doivent encore être spécifiées. Les compositions sont principalement données en tant que composante des matériaux (rupture de molen), X Pour la phase liquide et et Pour la phase de vapeur. Un équilibre de liquide de vapeur existe dans la zone entre le triple et le point critique. La pression, qui est réglée ou réglée dans l’équilibre du liquide de vapeur, est appelée pression de vapeur de saturation.
Les poids de mélange-vapeur-fluide-égal se caractérisent par le fait que la composition de la phase liquide et en forme de vapeur diffère généralement. Cet effet découle de la volatilité différente et donc de la pression partielle différente des substances impliquées et est utilisée dans les procédures de séparation, en particulier la rectification pour séparer les mélanges. Le pichet encastré s’enrichit en phase de vapeur, mais le schwersieder, en revanche, en phase liquide. La rectification est actuellement le processus le plus fréquemment utilisé pour la séparation des tissus, par exemple dans les raffineries d’huile. Les systèmes dans lesquels la composition ne diffère pas sont appelés acotropes et ne peuvent pas être séparés par évaporation.
Primordial [ Modifier | Modifier le texte source ]]
Un certain nombre de paramètres ont été définis pour décrire l’équilibre à vapeur-liquide d’un mélange:
- Facteur de séparation qui décrit le rapport des pressions de vapeur de saturation des composants impliqués
- K facteur qui décrit le rapport des parts de tissu d’un composant en vapeur et liquide
- Volatilité relative qui décrit le rapport de deux k facteurs
Ces chiffres clés sont tous utilisés pour être en mesure de reconnaître de manière simple si la rectification doit être effectuée de manière raisonnable.

Les poids purs en tissu-égal sont généralement affichés comme des diagrammes de pression de température, mais souvent le logarithme de la pression est appliqué à la valeur de retour de la température, car cet affichage entraîne une ligne droite.
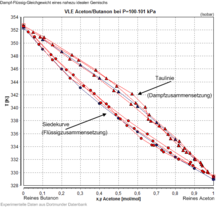
Les poids de fluide-fluide du mélange sont généralement déterminés expérimentalement à une température constante ou une pression constante. Par conséquent, les mélanges binaires VLE sont généralement représentés comme une température contre la composition et à une température constante comme pression contre la composition dans la phase liquide et vapeur. Les informations de concentration dans la vapeur sont appelées Toulinia, tandis que la séquence de compositions liquides est connue sous le nom de ligne de réglage. Une représentation alternativement commune est l’application des deux compositions dans le liquide et la vapeur X contre Y.
Un équilibre fluide en tissu pur peut être décrit par des équations simples dérivées de l’équation de Clausius Clapeyon, comme l’équation d’Antoine. Ces équations utilisent des paramètres spécifiques au tissu qui ont été adaptés aux données expérimentales de pression de vapeur.
Un équilibre de fluide de vapeur de mélange peut être décrit dans la première approximation par la loi Raoults. Cependant, cela nécessite le comportement idéal des substances impliquées. Pour prendre en compte le comportement réel, les modèles de coefficient d’activité tels que le modèle non aléatoire-two-liquide (NRTL) ou Uniquac (universel quasichémique) sont utilisés pour décrire l’énergie excessive gibbienne. La méthode UNIFAC convient pour estimer les coefficients d’activité.
- Dechema Chemistry Data Series, bande 1, collection de données d’équilibre vapeur-liquide, diverses autoren.
- «Les propriétés des gaz et des liquides», Bruce E. Poling, John M. Prausnitz, John P. O’Connell, McGraw-Hill Professional, 2000, ISBN 0-07-011682-2
- Perry, R.H. et Green, D.W. «Perry’s Chemical Engineers ‘Handbook», 7. Auflage, McGraw-Hill, 1997, ISBN 0-07-049841-5
- Henry-Law
- Base de données de Dortmund (collecte de données d’équilibre à vapeur des mélanges et de saturation de vapeur de tissus purs, base de la série de données de chimie DeChema))
Recent Comments