Corps Keto – Wikipedia
| Corps cétone (exemples) |
|---|
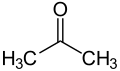 Acéton |
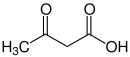
Acide 3-céto-boutique |

( R ) -3 acide de beurre hydroxy |
Corps cétone ou Ket est le dessin collectif pour trois connexions, qui se forment principalement dans le métabolisme catabolique (c.-à-d. La faim, le régime de réduction ou un régime faible en glucides) et peut conduire à la cétose. Sous les corps cétone, vous résumez l’acétoacétate (également appelé acétacéta), l’acétone et le β-hydroxybutyrat ou le 3-hydroxybutyrat. Cette dernière connexion est la plus importante des trois.
Les corps cétone sont formés dans le foie en acétyl-CoA, qui provient de la β-oxydation. Ils représentent une forme transportable des acétyl CoAs dans le corps humain. Pour utiliser les corps cétone, le cerveau et les muscles doivent d’abord changer en exprimant des enzymes nécessaires pour réchanger les corps cétone dans l’acétyl-CoA. Dans les temps de faim, les corps cétone contribuent une part considérable de la production d’énergie. Après un certain temps, il est possible que le cerveau s’entende avec 40 grammes au lieu de 120 grammes de glucose par jour.
Kétogénies [ Modifier | Modifier le texte source ]]
La synthèse du corps de cétone est composée de deux molécules acides acétiques activées, acétyl-CoA, le produit intermédiaire normal de la dégradation des acides gras. Premièrement, l’acétyl-coa-acétyltransférase est formée par l’acétoacétyl CoA, qui est étendue en utilisant une autre unité acétyl CoA et l’enzyme HMG COA synthase synthase en intermédiaire 3-hydroxy-3-méthyl-glutaryl-CoA (HMG-CoA). Enfin, le HMG CoA-Lyase se divise de l’acétoacétate. Ces trois étapes se déroulent exclusivement dans les mitochondries du foie (cycle de Lynen). Le 3-hydroxybutyrat se produit enfin dans le cytosol à travers le D -β-hydroxybutyrat – déshydrogénase.
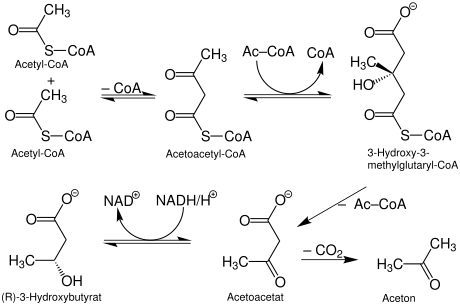
Le HMG-CoA est également un produit final dans la dégradation de la leucine à l’acide aminé, l’acétoacétate survient lorsque les acides aminés phénylalanine et la tyrosine.
La décarboxylation spontanée crée de l’acétone d’acétone; Il est parfois perçu dans le souffle des diabétiques et du régime alimentaire. Il ne peut être utilisé que par le corps dans une mesure limitée à la gluconéogenèse [d’abord] . Cependant, la proportion d’acétone dans les corps de cétone est faible.
Métabolisme [ Modifier | Modifier le texte source ]]
Hors de D -β-hydroxybutyrat peut être obtenu à l’aide de l’enzyme 3-hydroxybutyryrat déshydrogénase acétoacétate; La réaction est facilement réversible. L’acide à 3-cétonières-CoA transfère du COA en acétoacétate, tandis que le succinate est libérée en même temps. En fin de compte, l’acétyl-CoA est obtenu deux fois à partir de l’acétoacétyl CoA et du COA; La catalyse de cette réaction s’occupe de l’acétyl-coa-acétyltransférase, également l’inversion d’une réaction qui se déroule pendant la synthèse.
Cette activation des corps cétone a lieu dans la matrice mitochondriale de toutes les cellules qui peuvent traiter les corps cétone, mais pas dans le foie. Enfin, l’acétyl-CoA obtenu de cette manière se déroule dans le cycle Citratz, où l’énergie est obtenue à partir de l’oxydation.
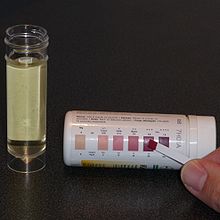
Avec le diabète sucré de type 1 (diabète), les corps cétone dans l’urine (Kétonurie) se trouvent en cas de manque absolu d’insuline. Ceci est basé sur une concentration excessive de celui-ci dans le sang. Comme le glucose, le rein laisse les corps de cétone à l’écart d’une concentration de sang accrue.
La raison de l’augmentation de la production du corps cétone est le manque d’insuline: bien qu’il y ait en fait suffisamment de glucose dans le sang, il ne peut pas entrer dans les cellules sans insuline, car l’installation de braises dans les membranes plasmiques des cellules musculaires squelettiques et des adipocytes ne peut pas être déposée sans insuline [2] . Par conséquent, malgré une augmentation de la glycémie dans le sang dans les cellules, il y a un manque de glucose. Cela conduit à la dégradation de la graisse (lipolyse) pour la production d’énergie. Alors que l’insuline inhibe le démantèlement de la graisse du dépôt, la carence en insuline favorise la perte de graisse et la lipolyse. Une lipolyse induite par un faible niveau d’insuline est typique du métabolisme de la faim. Les corps cétone sont formés si le produit de dégradation des acides gras, l’acétyl-CoA, ne peut pas entrer dans le citratzycle en raison d’une concentration trop petite oxalacet. L’oxalacétate peut être synthétisé dans une réaction anaplérotique de Pyruvat. Le pyruvat est le produit final de la glycolyse. Le faible niveau de glucose dans le cas du diabète sucré dans les cellules conduit à de petites quantités de pyruvat et donc à de petites quantités d’oxalacétate, ce qui favorise la formation de cétone à partir de l’acétyl-CoA. Dans le cas de trop de corps cétone dans le sang, son pH baisse et il y a une cétoacidose, qui conduit dans le pire des cas à un coma cétoacidotique. C’est pourquoi cela ne se produit généralement qu’avec le diabète sucré de type 1, car il y a une carence en insuline absolue ici. Dans le diabète de type 2 avec une carence relative à l’insuline, le corps a formé une résistance à l’insuline, qui forme de plus en plus de l’insuline. Avec cet effet d’insuline, quoique réduit, bien que le corps peut éviter la formation de corps cétone.
Un symptôme typique de la cétose est l’odeur de l’acétone (dissolvant de vernis à ongles) dans l’air que nous respirons, car le corps cétone est expiré sur eux.
Dans le cas d’une hypoglycémie persistante avec un nombre à faible teneur en cétone dans le sang, la présence d’un trouble d’oxydation des acides gras doit cependant être envisagée. Un exemple de ceci est une carence en coa-coa déshydrogénase à chaîne moyenne.
- Mountain / Tymoczko / Stryer: Biochimie . 5e édition, Spektrum Akademischer Verlag GmbH, Heidelberg 2003, ISBN 3-8274-1303-6.
- ↑ J. P. Casazza, M. E. Felver, R. L. Veech: Le métabolisme de l’acétone chez le rat . Dans: Le Journal of Biological Chemistry . Groupe 259 , Non. d’abord , 10 janvier 1984, S. 231–236 , PMID 6706932 .
- ↑ Löffler, Petrides: Biochimie et pathobiochemistrie . Ed.: Heinrich, Müller, Graeve. 9. Édition. Springer, 2014, ISBN 978-3-642-17972-3, S. 154 .
Recent Comments