P-V-T-T-T-Diagramm – Wikipedia
UN Diagramme P-V-T En chimie physique et thermodynamique, la représentation à trois dimensions des états d’un système thermodynamique avec la pression des variables d’état p , volume spécifique dans et la température T . De un tel Diagramme de condition L’état d’équilibre thermodynamique du système peut être lu dans les conditions données. Si le système peut se produire dans divers états agrégés, leurs domaines d’existence respectifs peuvent être trouvés dans le diagramme. Dans ce contexte, le diagramme est également utilisé comme Diagramme de phase désigné.
Comme le montre l’expérience, l’état d’une phase fluide d’un tissu pur (ou un mélange fluide avec composition constante) est clairement défini en spécifiant deux variables d’état intensives indépendantes et une taille d’état étendue. [d’abord] La taille étendue de l’état contient la quantité de matériel du système considéré. Si son montant n’est pas important, les deux variables d’état intensives restantes sont suffisantes pour déterminer clairement l’état du système. À cette fin, par exemple, les tailles mesurables peuvent être spécifiquement en volume dans et la température T pour être voté. Cette paire de valeurs est ensuite clairement attribuée à un point sur la zone de l’État, qui comprend une certaine pression. Le volume spécifique associé résulte également du choix d’une paire de valeurs.
Ce diagramme à trois dimensions offre une présentation claire des différentes conditions, mais ne convient pas à la saisie des données en béton.
Cependant, les projections de ce diagramme en trois niveaux (niveau P-V, niveau P-T et niveau T-V) sont des diagrammes de travail très utilisés, car les valeurs peuvent être lues sur les coordonnées. Le plus connu est le diagramme P-V.
Selon la taille intensive V, la taille étendue V est également utilisée selon les besoins, par exemple pour le processus dans un moteur de piston avec certaines dimensions de cylindre.

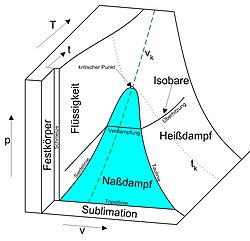
Puisque, comme indiqué dans les deux illustrations, le comportement de condition des tissus ou des mélanges de tissu est généralement indiqué dans les trois phases (états d’agrégation “ferme”, “liquide” et “gazeux”) P-V-T -Diagramme et ses projections également appelées diagrammes de phase.
Un tel diagramme de phase contient généralement
- Zones dans lesquelles il n’y a qu’une seule phase dans laquelle l’ensemble du système est, par exemple, ferme ou liquide.
- Zones dans lesquelles deux phases différentes se produisent ensemble, dans lesquelles le système a été à moitié fondu, par exemple. La pression indiquée dans le diagramme est alors les deux phases de la pression d’équilibre commune, par exemple la pression de vapeur dans un système qui se compose d’un liquide et d’une phase gazeuse. Les deux phases ont également la même température.
- Une zone (ligne de triplé) dans laquelle les trois phases peuvent coexister ensemble. Les trois phases ont la même pression et la même température (avec de l’eau 0,01 ° C et 611,657 ± 0,010 PA).
Le point critique est l’état dans lequel la ligne de réglage et la Tulinia sont effondrés. Dans le cas de l’apport de chaleur isobare avec une pression critique (pour l’eau 221,2 bar) – et au-dessus – la phase liquide entre dans la phase gazeuse sans processus d’évaporation (l’isobar ne passe pas par la zone de vapeur humide).
- Le P-V-T -GRAM est la représentation graphique de l’équation de condition thermique du système, qui également les variables p , dans et T utilisé pour la description de la condition.
- ↑ HAUTE DÉFINITION. Baehr: Thermodynamique. 12. Edition, Springer, Berlin / Heidelberg / New York 2005, ISBN 3-540-23870-0, p. 20.
Recent Comments