Joseph John Thomson – Wikipedia

Zdjęcie po 1916 roku.
Suplementy

Joseph John Thomson , urodzony i martwy , jest brytyjskim fizykiem.
Odkrył elektron, a także izotopy i wynalazł spektrometrię mas; Przeanalizował rozprzestrzenianie się fal przewodniczych.
Otrzymał nagrodę Nobla w 1906 roku w dziedzinie fizyki „Jego teoretyczne i eksperymentalne badania dotyczące przewodnictwa elektrycznego w gazach [[[ Pierwszy ] » . Badanie to dostarczyło dowodów na istnienie elektronu.

Joseph John Thomson urodził się z Szkoccy rodzice [Ref. niezbędny] na wzgórzu Cheetham na przedmieściach Manchesteru . W 1870 r. Rozpoczął studia inżynierskie na University of Manchester, znanym wówczas jako Owens College, wówczas w 1876 r., Wszedł do Trinity College w Cambridge. . , poślubił Rose Elizabeth Paget [[[ notatka 1 ] Który był badaczem w Cavendish Laboratory. Mieli dwoje dzieci, Joan Paget Thomson i George Paget Thomson, przyszły zwycięzca Nagrody Nobla w dziedzinie fizyki w 1937 roku. W 1884 r. Zastąpił lorda Rayleigh na krześle Cavendish w Experimental Physics [[[ 2 ] . W tym samym roku Thomson został członkiem Royal Society .
W 1902 roku otrzymał Medal Hughesa w 1906 r. Nagroda Nobla w dziedzinie fizyki za pracę nad przewodnictwem elektrycznym gazów [[[ Pierwszy ] oraz w 1914 r. Medal Copley. W 1908 r. Został członkiem Zakonu Merit [[[ 3 ] , co daje mu prawo do tytułu Pan .
Jest prezydentem Royal Society W latach 1916–1920. W 1919 r. Jeden z jego studentów, Ernest Rutherford, zastąpił go na przewodniczącego Cavendish w fizyce eksperymentalnej. Zmarł W Cambridge i jest pochowany w opactwie Westminster.
W 1897 r. Thomson udowadnia eksperymentalnie istnienie elektronów, które zostały przewidziane przez George’a Johnstone Stoney w 1874 roku.
To odkrycie jest wynikiem szeregu doświadczeń na półkach katodowych.
W tym samym roku przedstawił swój model atomu, model budyń śliwkowych.
Pierwsze doświadczenie [[[ modyfikator |. Modyfikator i kod ]
W swoim pierwszym doświadczeniu bada możliwość oddzielenia ujemnego obciążenia elektrycznego od promieni katodowych przez magnetyzm.
Buduje rurkę katodową, która kończy się parą cylindrów z szczelinami podłączonymi do elektrometru.
Thomson odkrywa, że jeśli promienie katodowe są odchylone przez pole magnetyczne, aby nie mogły wejść przez szczeliny, elektrometr prawie nie rejestruje obciążenia elektrycznego. Dochodzi do wniosku, że obciążeniem ujemnym nie można oddzielić od półek.
Drugie doświadczenie [[[ modyfikator |. Modyfikator i kod ]

W swoim drugim doświadczeniu pokazuje, że promienie katodowe można odchylić przez pole elektryczne, które można przewidzieć dla obciążonych cząstek. Rzeczywiście, inni badacze bez powodzenia próbowali obserwować ten efekt, ale Thomson uważa, że poprzednie doświadczenia były błędne z powodu śladów gazu.
Buduje katodową rurkę z bardziej obszerną pustką, a na końcu wyposaża warstwę farby fosforescencyjnej, aby wykryć promienie padające.
Thomson pokazuje odchylenie w jednym kierunku, co wskazuje, że obciążenie promieni katodowych jest ujemne.
Trzecie doświadczenie [[[ modyfikator |. Modyfikator i kod ]
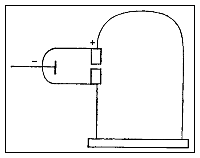
W trzecim doświadczeniu Thomson określa stosunek obciążenia masowego (E/M) promieni katodowych poprzez pomiar ich odchylenia pod wpływem pola magnetycznego, a także energii kinetycznej. Oblicza E/M tysiące razy wyższy niż podobny stosunek dla jonu wodoru (h + ), co sugeruje, że promienie katodowe zawierają cząstki bardzo lekkie lub bardzo wysoko załadowane.
Thomson dochodzi do odważnego wniosku: promienie katodowe składają się z „ciałek”, które pochodzą z wnętrza atomów elektrod, co implikuje, że atomy są podzielne. „Corpusle” odkryte przez Thomsona to elektron dostarczony już przez Stoney.
Thomson wyobraża sobie model atomu „śliwkowego budyń”, do którego te ciałki (śliwki) poruszają się w morzu o dodatnich obciążeniach (podding). Jednak pomysł ten jest później zaprzeczony przez Ernesta Rutherforda, który pokazuje, że obciążenie dodatnie jest skoncentrowane w jądrze.
Odkrycie elektronu zostało ogłoszone Przed instytucją królewską [[[ 4 ] I spowodował wrażenie w świecie naukowym. W 1906 roku Thomson otrzymał Nagrodę Nobla w dziedzinie fizyki [[[ Pierwszy ] .
Inne badania: izotopy i spektrometria masowa [[[ modyfikator |. Modyfikator i kod ]
W 1906 r. Thomson wykazał, że atom wodoru zawierał tylko jeden elektron. W tym czasie niektóre teorie rozważały różną liczbę elektronów.
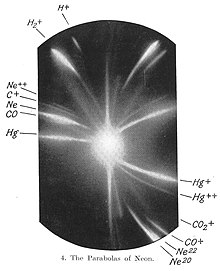
W 1912 r. Badał skład mieszanin „jonów anodowych” SO. Podczas tych badań mierzy ugięcie jonizowanej wiązki neonowej ( + ), który przechodzi przez pole magnetyczne, a także pole elektryczne. Na płycie fotograficznej, która służy mu jako detektora, obserwuje dwa miejsca (patrz obraz), które odpowiadają atomom mas 20 i 22. Stwierdza, że neon składa się z atomów dwóch różnych mas lub izotopów.
To oddzielenie atomów przez ich masę jest pierwszym przykładem spektrometrii mas, metody, która następnie opracowała Francis William Aston (student Thomson) i Arthur Jeffrey Demptter.
- 1883: Traktat o ruchu pierścieni wiru , University of Cambridge, Londres (ISBN 0-543-95696-2 ) .
- 1888: Zastosowania dynamiki do fizyki i chemii Londyn. (ISBN 1-4021-8397-6 ) .
- 1893: Uwagi na temat ostatnich badań w zakresie energii elektrycznej i magnetyzmu , Oxford University Press, 1991. (ISBN 1-4297-4053-1 ) .
- 1895: Elementy matematycznej teorii elektryczności i magnetyzmu Londyn.
- 1897: Promienie katodowe , Postępowanie instytucji królewskiej.
- 1897: Promienie katodowe , Magazyn filozoficzny.
- 1901: Podręcznik fizyki w pięciu tomach , Co -Wpisanie z J.H. Poyntingiem.
- 1903: Przewodzenie energii elektrycznej przez gazy , Cambridge University Press (drugie bardziej kompletne wydanie w 1906 r.).
- 1904: Na strukturze atomu .
- 1912: Dalsze eksperymenty dotyczące promieni pozytywnych .
- 1912: Przejście energii elektrycznej przez gazy , Gauthier-Villars (Paryż) Tekst online dostępny na IRIS .
- 1913: Promienie dodatniego energii elektrycznej , Proceedings of the Royal Society.
- 1922: Elektryczność i materiał , Przedmowa Paula Langevina.
- 1923: Elektron w chemii , Filadelfia.
Notatki [[[ modyfikator |. Modyfikator i kod ]
- Córka Sir George E. Paget.
Bibliografia [[[ modyfikator |. Modyfikator i kod ]
- (W) ‘ W uznaniu wielkich zalet jego teoretycznych i eksperymentalnych badań dotyczących przewodzenia energii elektrycznej przez gaz » W Kadra edytorska, ” Nagroda Nobla w dziedzinie fizyki 1906 », Nobel Foundation, 2010. Dostęp 13 czerwca 2010 r.
- Cavendish profesor fizyki eksperymentalnej .
- London Gazette : N O 28206, P. 9650 , 18-12-1908.
- (W) Harald Fritzsch, Cząstki elementarne: elementy budulcowe materii , Światowy nauk, W P. dwunasty .
Powiązane artykuły [[[ modyfikator |. Modyfikator i kod ]
Linki zewnętrzne [[[ modyfikator |. Modyfikator i kod ]
- (W) Biografia Na stronie Nobel Foundation (opaska na stronie zawiera kilka linków dotyczących ceremonii wręczenia nagród, w tym dokument napisany przez zwycięzcę – Wykład Nobla – który szczegółowo opisuje jej wkład)
-
Uwagi w słownikach ogólnych lub encyklopediach :
- Zasoby badawcze :
- Zasoby dzieł sztuki :
Recent Comments