Transalkylation – wikipedia wiki
Un article de Wikipédia, l’encyclopédie libre
Réaction chimique qui transfère un groupe alkyle entre les molécules
Chimie inorganique, transalkylation est une réaction chimique impliquant le transfert d’un groupe alkyle d’un composé organique à un autre. La réaction est utilisée pour le transfert de groupes méthyle et éthyle entre les anneaux de benzène. C’est d’une valeur particulière dans l’industrie pétrochimique [d’abord] Pour fabriquer du p-xylène, du styrène, [2] et d’autres composés aromatiques. La motivation pour l’utilisation des réactions de transalkylation est basée sur une différence de production et de demande de benzène, de toluène et de xylènes. La transalkylation peut convertir le toluène, qui est surproduit, en benzène et xylène, qui sont sous-produits. [3] Les zéolites sont souvent utilisées comme catalyseurs dans les réactions de transalkylation. [4]
Disproportionnement [ modifier ]]

Réaction du toluène pour produire du benzène et du xylène
La transalkylation, telle qu’elle est utilisée par l’industrie pétrochimique, est souvent utilisée pour convertir le toluène en benzène et xylènes. Ceci est réalisé grâce à une réaction de disproportionnement du toluène dans lequel une molécule de toluène transfère son groupe méthyle à un autre. La réaction n’est pas sélective et le xylène produit peut être ortho, méta ou par. Il y a une demande plus élevée de para xylène, il est donc souvent séparé, et le mélange est autorisé à rééquilibrer pour donner plus de para produit. [3]
Diéthylbenzènes [ modifier ]]
Les diéthylbenzènes surviennent en tant que produits latéraux de l’alkylation du benzène avec de l’éthylène, qui est effectué à très grande échelle. Puisqu’il n’y a qu’un marché limité pour le diéthylbenzène, une grande partie est recyclée par transalkylation pour donner de l’éthylbenzène: [d’abord]
- Rapport m / r [ modifier ]]
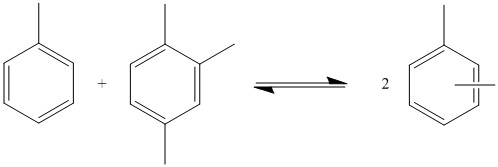 Transalkylation du toluène et du triméthylbenzène pour produire du xylène. Dans cet exemple, le rapport M / R est 2.
Transalkylation du toluène et du triméthylbenzène pour produire du xylène. Dans cet exemple, le rapport M / R est 2.Ce type de réaction peut également être effectué avec du toluène et du triméthylbenzène pour produire du xylène. La réaction se produit via l’équilibre, donc le produit n’est pas du xylène pur. De nombreux produits sont produits avec un nombre variable de groupes méthyle. Les quantités dans lesquelles chaque produit est produit dépend du rapport M / R. Il s’agit du rapport du nombre de groupes méthyle au nombre de bagues de benzène dans tous les substrats. Par exemple, dans la disproportionnement du toluène, le rapport M / R est 1. les réactions secondaires dans lesquelles les alcanes sont produits réduisent le nombre de groupes méthyle disponibles qui diminuent le rapport M / R. Cela peut être atténué en ajoutant des composés avec un nombre plus élevé de groupes méthyle, tels que le triméthylbenzène. Le rapport des produits produits ne dépend que du rapport M / R afin que différents matériaux de départ puissent produire les mêmes composés via la transalkylation. [3]
Catalyseurs de zéolite [ modifier ]]
Des réactions de transalkylation de six à dix aromatiques méthylées en carbone sont souvent réalisées avec le COFED d’hydrogène gazeux, sur un catalyseur solide à base de zéolite. Les processus industriels exploitent le réacteur de transalkylation à une température et une pression élevées pour atteindre l’économie des processus souhaitée. Les zéolites sont des solides micro-cristallins composés de tétraédriques Alo
4 et Ce n’est pas
4 blocs de construction. Ces cristaux sont de nature poreuse avec des canaux micropores caractéristiques, des cavités. La zéolite est connue comme une classe de tamis moléculaire en raison de leurs ouvertures de canal se situe souvent entre 0,4 à 1,5 nanomètres, juste assez pour que les molécules passent. Les molécules aromatiques entrent et quittent ces canaux à différents taux, également appelés diffusion. En plus de leur effet de tamisage moléculaire, les zéolites ont une faible liaison des protons provenant de sa composition chimique. Ce sont des centres chimiques actifs pour une réaction de transalkylation catalysée par l’acide.Des zéolites de tailles variables sont utilisées pour effectuer une transalkylation sur différents substrats. Par exemple, les zéolites avec une taille de pore de 5,5 Å conviennent aux transalkylations de benzène, de toluène, de xylènes et de triméthylbenzènes. [5] [3] [6]
Phénols [ modifier ]]
La transalkylation est utilisée dans la production commerciale d’aromatiques au-delà des matières premières BTX habituelles. Par exemple, 4- se terminer -Butylphénol est produit en partie via deux réactions de transalkylation. [7] Dans un exemple, se terminer -Le éther de butylphényle est isomérisé au phénol:
- [8]
 Le 1,3-diisopropylbenzène est produit par transalkylation.
Le 1,3-diisopropylbenzène est produit par transalkylation.Voir également [ modifier ]]
Les références [ modifier ]]
- ^ un b Griesbaum, Karl; Behr, Arno; Bid, Dieter; Voges, Heinz-Wanderer; Garbe, Dorothea; Paetz, Christian; Collin, Gerd; Mayer, Dieter; Höke (2000). “Hydrocarbures”. Encyclopédie de la chimie industrielle d’Ullmann . Weinheim: Wiley-VCH. Est ce que je: 10.1002 / 14356007.A13_227 .
- ^ Processus de styrène avec recyclage de la zone de déshydrogénation Archivé 2012-03-20 sur la machine Wayback
- ^ un b c d TSAI, TSENG-CHANG “Disproportionation et transalkylation des alkylbenzènes sur les catalyseurs de zéolite”. Elsevier Science, 1999
- ^ Application américaine 20100022814 , Goncalvez de Almeida; Jose Luis & Berna Tejero et al., “Catalytic Transalkylation of Dialkyl Benzènes”, publié 2010-01-28, affecté à Petroquimica Espanola, S.A. Petresa
- ^ Harmer, Mark A.; Sun, Qun (2001). “Catalyse d’acide solide à l’aide de résines d’échange d’ions”. Catalyse appliquée A: Général . 221 (1–2): 45–62. est ce que je: 10.1016 / S0926-860X (01) 00794-3 .
- ^ Al-Khattaf, Sulaiman; Ali, Syed A.; Aitani, Abdullah M.; Žilková, Naděžda; Kubička, David; Čejka, Jiří (2014). “Advanceces récentes en réaction des alkylbenzènes sur de nouveaux zéolithes: les effets de la structure et de la morphologie de la zéolite”. Revues de catalyse . 56 (4): 333–402. est ce que je: 10.1080 / 01614940.2014.946846 . S2cid 97415930 .
- ^ Fiege, Helmut; Voges, Heinz-Werner; Hamamoto, Toshikazu; Umemura, Sumio; Iwata, Tadao; Miki, Hisaya; Fujita, Yasuhiro; Buysch, Hans- Josef; Garbe (2000). “Dérivateurs de phénol”. Encyclopédie de la chimie industrielle d’Ullmann . Weinheim: Wiley-VCH. Est ce que je: 10.1002 / 14356007.A19_313 .
- ^ K. W. Message, D. Decker (2012). “Resorcinol”. Encyclopédie de la chimie industrielle d’Ullmann . Weinheim: Wiley-VCH. Est ce que je: 10.1002 / 14356007.A23_111.pub2 .
{{cite Encyclopedia}}: CS1 MAINT: utilise le paramètre des auteurs (lien)
Liens externes [ modifier ]]
- [8]


 [8]
[8]
Recent Comments