
Polyetylen hoặc polythene (viết tắt PE ; tên IUPAC polyethene hoặc poly (methylene) nhựa. Tính đến năm 2017 [update]hơn 100 triệu tấn nhựa polyetylen được sản xuất hàng năm, chiếm 34% tổng thị trường nhựa. [5][6] Công dụng chính của nó là trong bao bì (túi nhựa, màng nhựa, màng địa chất, hộp đựng, kể cả chai, v.v.) Nhiều loại polyetylen được biết đến, với hầu hết có công thức hóa học (C 2 H 4 ) n . PE thường là hỗn hợp các polyme tương tự ethylene với các giá trị khác nhau của n . Polyetylen là một loại nhựa nhiệt dẻo; tuy nhiên, nó có thể trở thành nhựa nhiệt rắn khi được sửa đổi (chẳng hạn như polyetylen liên kết ngang).
Lịch sử [ chỉnh sửa ]
Polyetylen lần đầu tiên được tổng hợp bởi nhà hóa học người Đức Hans von Pechmann, người đã điều chế nó một cách tình cờ vào năm 1898 khi điều tra diazomethane. [7][8] và Friedrich Tschirner đã mô tả chất trắng, sáp mà anh ta đã tạo ra, họ nhận ra rằng nó chứa LongCHCH 2 – chuỗi và gọi nó là polymylene . [9]

Sự tổng hợp polyetylen thực tế công nghiệp đầu tiên (diazomethane là một chất không ổn định nổi tiếng thường được tránh trong ứng dụng công nghiệp) được phát hiện vào năm 1933 bởi Eric Fawcett và Reginald Gibson, một lần nữa tai nạn, tại Công ty hóa chất hoàng gia (ICI) hoạt động ở Northwich, Anh. [10] Khi áp dụng áp suất cực cao (vài trăm khí quyển) vào hỗn hợp ethylene và benzaldeh yde họ lại sản xuất một vật liệu sáp trắng. Bởi vì phản ứng đã được bắt đầu bằng ô nhiễm oxy trong thiết bị của họ, nên ban đầu, thí nghiệm này rất khó sinh sản. Mãi đến năm 1935, một nhà hóa học ICI khác, Michael Perrin, đã phát triển tai nạn này thành một tổng hợp áp suất cao có thể tái tạo cho polyetylen trở thành cơ sở cho sản xuất polyetylen mật độ thấp (LDPE) công nghiệp bắt đầu vào năm 1939. Bởi vì polyetylen được tìm thấy tính chất tổn thất thấp ở sóng vô tuyến tần số rất cao, phân phối thương mại ở Anh đã bị đình chỉ khi Chiến tranh thế giới thứ hai bùng nổ, áp đặt bí mật và quy trình mới được sử dụng để sản xuất cách điện cho cáp đồng trục UHF và SHF của các bộ radar. Trong Thế chiến II, nghiên cứu sâu hơn đã được thực hiện về quy trình ICI và vào năm 1944 Bakelite Corporation tại Sabine, Texas và Du Pont tại Charleston, West Virginia, đã bắt đầu sản xuất thương mại quy mô lớn theo giấy phép từ ICI. [11]
việc sản xuất polyetylen thương mại bắt đầu với sự phát triển của chất xúc tác thúc đẩy quá trình trùng hợp ở nhiệt độ và áp suất nhẹ. Đầu tiên trong số này là chất xúc tác dựa trên crom trioxide, được phát hiện vào năm 1951 bởi Robert Banks và J. Paul Hogan tại Phillips Dầu khí. [12] Năm 1953, nhà hóa học người Đức Karl Ziegler đã phát triển một hệ thống xúc tác dựa trên các hợp chất halogen và hợp chất organoaluminium hoạt động tại thậm chí điều kiện nhẹ hơn chất xúc tác Phillips. Tuy nhiên, chất xúc tác Phillips ít tốn kém hơn và dễ làm việc hơn, và cả hai phương pháp đều được sử dụng nhiều trong công nghiệp. Đến cuối những năm 1950, cả hai chất xúc tác loại Phillips và Ziegler đã được sử dụng để sản xuất HDPE. Vào những năm 1970, hệ thống Ziegler đã được cải thiện nhờ sự kết hợp của magiê clorua. Các hệ thống xúc tác dựa trên các chất xúc tác hòa tan, các kim loại, đã được báo cáo vào năm 1976 bởi Walter Kaminsky và Hansjorg Sinn. Các họ xúc tác dựa trên Ziegler và metallicocene đã được chứng minh là rất linh hoạt trong việc đồng trùng hợp ethylene với các olefin khác và đã trở thành cơ sở cho nhiều loại nhựa polyetylen hiện có, bao gồm polyetylen mật độ rất thấp và polyetylen mật độ thấp tuyến tính. Các loại nhựa này, dưới dạng sợi UHMWPE, đã bắt đầu (kể từ năm 2005) bắt đầu thay thế aramids trong nhiều ứng dụng cường độ cao.
Thuộc tính [ chỉnh sửa ]
Các tính chất của polyetylen có thể được chia thành các tính chất cơ học, hóa học, điện, quang học và nhiệt. [13]
Tính chất cơ học của polythene chỉnh sửa ]
Polyetylen có độ bền, độ cứng và độ cứng thấp, nhưng có độ dẻo và độ bền va đập cao cũng như ma sát thấp. Nó cho thấy creep mạnh dưới lực liên tục, có thể giảm bằng cách thêm các sợi ngắn. Nó cảm thấy như sáp khi chạm vào.
Tính chất nhiệt [ chỉnh sửa ]
Khả năng ứng dụng thương mại của polyetylen bị giới hạn bởi điểm nóng chảy tương đối thấp. Đối với các loại thương mại phổ biến của polyetylen trung bình và mật độ cao, điểm nóng chảy thường nằm trong khoảng 120 đến 180 ° C (248 đến 356 ° F). Điểm nóng chảy của polyetylen trung bình, thương mại, mật độ thấp thường là 105 đến 115 ° C (221 đến 239 ° F). Những nhiệt độ này thay đổi mạnh mẽ với các loại polyetylen.
Tính chất hóa học [ chỉnh sửa ]
Polyetylen bao gồm các hydrocacbon không phân cực, có trọng lượng phân tử cao. Do đó, hành vi hóa học của nó tương tự như parafin. Các đại phân tử riêng lẻ không liên kết cộng hóa trị. Do cấu trúc phân tử đối xứng của chúng, chúng có xu hướng kết tinh; tổng thể polyetylen là một phần tinh thể. Độ kết tinh cao hơn làm tăng mật độ và sự ổn định cơ học và hóa học.
Hầu hết các loại LDPE, MDPE và HDPE đều có khả năng kháng hóa chất tuyệt vời, nghĩa là chúng không bị axit mạnh hoặc bazơ mạnh tấn công và chống lại các chất oxy hóa và chất khử nhẹ. Các mẫu tinh thể không hòa tan ở nhiệt độ phòng. Polyetylen (trừ polyetylen liên kết ngang) thường có thể được hòa tan ở nhiệt độ cao trong các hydrocacbon thơm như toluene hoặc xylene, hoặc trong các dung môi clo hóa như trichloroethane hoặc trichlorobenzene. [14] [1993010] không có nước. Độ thấm khí và hơi nước (chỉ khí cực) thấp hơn so với hầu hết các loại nhựa; mặt khác, oxy, carbon dioxide và hương liệu có thể vượt qua nó một cách dễ dàng.
PE có thể trở nên giòn khi tiếp xúc với ánh sáng mặt trời, muội than thường được sử dụng làm chất ổn định tia cực tím.
Polyetylen cháy chậm với ngọn lửa màu xanh có đầu màu vàng và tỏa ra mùi parafin (tương tự như ngọn lửa nến). Vật liệu này tiếp tục cháy khi loại bỏ nguồn lửa và tạo ra một giọt nhỏ giọt. [15]
Polyetylen không thể được in hoặc liên kết bằng chất kết dính mà không cần tiền xử lý. Tham gia cường độ cao dễ dàng đạt được với hàn nhựa.
Tính chất điện [ chỉnh sửa ]
Polyetylen là một chất cách điện tốt. Nó cung cấp sức đề kháng cây điện tốt; tuy nhiên, nó trở nên dễ dàng tích điện (có thể giảm bằng cách bổ sung than chì, muội than hoặc chất chống tĩnh điện).
Tính chất quang học [ chỉnh sửa ]
Tùy thuộc vào lịch sử nhiệt và độ dày màng PE có thể thay đổi giữa gần như rõ ràng (trong suốt), mờ đục (mờ) hoặc mờ. LDPE do đó sở hữu lớn nhất, LLDPE ít hơn một chút và HDPE kém minh bạch nhất. Độ trong suốt bị giảm bởi các tinh thể nếu chúng lớn hơn bước sóng của ánh sáng khả kiến. [16]
Quá trình sản xuất polythene hoặc polyethylen [ chỉnh sửa ]
Monome [ chỉnh sửa ]
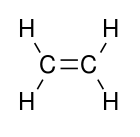

Ethylene (ethene)
Thành phần hoặc monome là ethylene (tên IUPAC ethene), một hydrocarbon dạng khí có công thức C 2 [19459] H 4 có thể được xem như là một cặp nhóm methylene (- CH
2 -) được kết nối với nhau. Thông số kỹ thuật điển hình là <5 ppm cho nước, oxy và các anken khác. Các chất gây ô nhiễm có thể chấp nhận bao gồm N 2 ethane (tiền chất phổ biến của ethylene) và metan. Ethylene thường được sản xuất từ các nguồn hóa dầu, nhưng cũng được tạo ra do mất nước ethanol. [14]
Polyme hóa [ chỉnh sửa ]
Ethylene là một phân tử khá ổn định chỉ trùng hợp khi tiếp xúc với các chất xúc tác. Việc chuyển đổi là tỏa nhiệt cao. Phối hợp trùng hợp là công nghệ phổ biến nhất, có nghĩa là sử dụng clorua kim loại hoặc oxit kim loại. Các chất xúc tác phổ biến nhất bao gồm titan (III) clorua, được gọi là chất xúc tác Ziegler-Natta. Một chất xúc tác phổ biến khác là chất xúc tác Phillips, được điều chế bằng cách lắng đọng oxit crom (VI) trên silica. [14] Polyetylen có thể được sản xuất thông qua phản ứng trùng hợp gốc, nhưng con đường này chỉ có công dụng hạn chế và thường yêu cầu thiết bị áp suất cao.
Tham gia [ chỉnh sửa ]
Các phương pháp thường được sử dụng để nối các bộ phận polyetylen với nhau bao gồm: [17]
Chất kết dính và dung môi hiếm khi được sử dụng vì polyetylen không phân cực và có khả năng kháng dung môi cao. Chất kết dính nhạy áp lực (PSA) là khả thi nếu hóa học bề mặt hoặc điện tích được sửa đổi bằng kích hoạt plasma, xử lý ngọn lửa hoặc xử lý corona.
Phân loại [ chỉnh sửa ]
Polyetylen được phân loại theo mật độ và phân nhánh. Tính chất cơ học của nó phụ thuộc đáng kể vào các biến như mức độ và loại phân nhánh, cấu trúc tinh thể và trọng lượng phân tử. Có một số loại polyetylen:
Liên quan đến khối lượng bán ra, các loại polyetylen quan trọng nhất là HDPE, LLDPE và LDPE.
Polyethylen có trọng lượng phân tử cực cao (UHMWPE) [ chỉnh sửa ]
UHMWPE là polyethylen trong hàng triệu, thường là từ 3,5 đến 7,5 triệu amu. [18] Trọng lượng phân tử cao làm cho nó trở thành một vật liệu rất cứng, nhưng dẫn đến việc đóng gói các chuỗi vào cấu trúc tinh thể kém hiệu quả bằng chứng là mật độ nhỏ hơn polyetylen mật độ cao (ví dụ: 0,930 cường0,935 g / cm 3 ). UHMWPE có thể được thực hiện thông qua bất kỳ công nghệ xúc tác nào, mặc dù các chất xúc tác Ziegler là phổ biến nhất. Do độ bền vượt trội và khả năng cắt, mòn và kháng hóa chất tuyệt vời, UHMWPE được sử dụng trong một loạt các ứng dụng. Chúng bao gồm các bộ phận máy xử lý chai và chai, bộ phận chuyển động trên máy dệt, vòng bi, bánh răng, khớp nhân tạo, bảo vệ cạnh trên sân băng, thay thế cáp thép trên tàu và thớt thịt. Nó thường được sử dụng để xây dựng các phần khớp của cấy ghép được sử dụng để thay thế khớp háng và khớp gối. Là sợi, nó cạnh tranh với aramid trong áo chống đạn.
Polyetylen mật độ cao (HDPE) [ chỉnh sửa ]

HDPE được xác định bởi mật độ lớn hơn hoặc bằng 0,941 g / cm 3 . HDPE có mức độ phân nhánh thấp. Các phân tử tuyến tính chủ yếu kết hợp với nhau tốt, vì vậy các lực liên phân tử mạnh hơn trong các polyme phân nhánh cao. HDPE có thể được sản xuất bởi các chất xúc tác crôm / silica, chất xúc tác Ziegler-Natta hoặc chất xúc tác luyện kim; bằng cách chọn các chất xúc tác và điều kiện phản ứng, một lượng nhỏ phân nhánh xảy ra có thể được kiểm soát. Các chất xúc tác này thích sự hình thành các gốc tự do ở phần cuối của các phân tử polyetylen đang phát triển. Chúng gây ra các monome ethylene mới để thêm vào đầu của các phân tử, thay vì dọc theo giữa, gây ra sự tăng trưởng của một chuỗi tuyến tính.
HDPE có độ bền kéo cao. Nó được sử dụng trong các sản phẩm và bao bì như bình sữa, chai chất tẩy rửa, bồn bơ, thùng đựng rác và ống nước. Một phần ba của tất cả các đồ chơi được sản xuất từ HDPE. Trong năm 2007, mức tiêu thụ HDPE toàn cầu đạt khối lượng hơn 30 triệu tấn. [19]
Polyetylen liên kết ngang (PEX hoặc XLPE) [ chỉnh sửa ]
PEX là phương tiện trung bình Polyetylen mật độ cao chứa các liên kết liên kết chéo được đưa vào cấu trúc polymer, thay đổi nhựa nhiệt dẻo thành nhiệt. Các đặc tính nhiệt độ cao của polymer được cải thiện, lưu lượng của nó bị giảm và khả năng kháng hóa chất của nó được tăng cường. PEX được sử dụng trong một số hệ thống ống nước có thể uống được vì các ống làm bằng vật liệu có thể được mở rộng để vừa với núm vú kim loại và nó sẽ từ từ trở lại hình dạng ban đầu, tạo thành một kết nối kín nước vĩnh viễn.
Polyetylen mật độ trung bình (MDPE) [ chỉnh sửa ]
MDPE được xác định bởi phạm vi mật độ 0,926 cách0,940 g / cm 3 . MDPE có thể được sản xuất bởi các chất xúc tác crom / silica, chất xúc tác Ziegler-Natta hoặc chất xúc tác luyện kim. MDPE có đặc tính chống sốc và rơi tốt. Nó cũng ít nhạy cảm hơn so với HDPE; ứng suất chống nứt tốt hơn nhựa HDPE. MDPE thường được sử dụng trong các ống dẫn khí và phụ kiện, bao tải, màng co, màng đóng gói, túi mang và đóng vít.
Polyetylen mật độ thấp tuyến tính (LLDPE) [ chỉnh sửa ]
LLDPE được xác định bởi phạm vi mật độ 0,915 Nott0.925 g / cm 3 . LLDPE là một loại polymer tuyến tính đáng kể với số lượng nhánh ngắn đáng kể, thường được tạo ra bằng cách đồng trùng hợp ethylene với alpha-olefin chuỗi ngắn (ví dụ, 1-butene, 1-hexene và 1-octene). LLDPE có độ bền kéo cao hơn LDPE, và nó thể hiện khả năng chống va đập và đâm thủng cao hơn LDPE. Có thể thổi các màng có độ dày thấp hơn, so với LDPE, với khả năng chống nứt ứng suất môi trường tốt hơn, nhưng không dễ xử lý. LLDPE được sử dụng trong bao bì, đặc biệt là màng cho túi và tấm. Độ dày thấp hơn có thể được sử dụng so với LDPE. Nó được sử dụng để bọc cáp, đồ chơi, nắp, xô, thùng chứa, và đường ống. Mặc dù các ứng dụng khác có sẵn, LLDPE được sử dụng chủ yếu trong các ứng dụng phim do độ bền, tính linh hoạt và độ trong suốt tương đối của nó. Ví dụ về sản phẩm bao gồm từ màng nông nghiệp, bọc Saran và bọc bong bóng, cho đến màng đa lớp và composite. Vào năm 2013, thị trường LLDPE trên thế giới đạt khối lượng 40 tỷ đô la Mỹ. [20]
Polyetylen mật độ thấp (LDPE) [ chỉnh sửa ]
LDPE được xác định bởi phạm vi mật độ 0,910. 0,940 g / cm 3 . LDPE có mức độ phân nhánh chuỗi ngắn và dài cao, điều đó có nghĩa là các chuỗi cũng không đóng gói vào cấu trúc tinh thể. Do đó, nó có lực liên phân tử ít mạnh hơn do lực hút lưỡng cực tức thời gây ra – lưỡng cực ít hơn. Điều này dẫn đến độ bền kéo thấp hơn và độ dẻo tăng. LDPE được tạo ra bằng cách trùng hợp gốc tự do. Mức độ phân nhánh cao với các chuỗi dài mang lại cho LDPE tính chất dòng chảy độc đáo và mong muốn. LDPE được sử dụng cho cả thùng cứng và các ứng dụng màng nhựa như túi nhựa và màng bọc. Năm 2013, thị trường LDPE toàn cầu có khối lượng gần 33 tỷ USD. [21]
Quá trình trùng hợp triệt để được sử dụng để tạo LDPE không bao gồm chất xúc tác "giám sát" các trang web triệt để trên " phát triển chuỗi PE. (Trong quá trình tổng hợp HDPE, các vị trí gốc nằm ở cuối chuỗi PE, vì chất xúc tác ổn định sự hình thành của chúng ở đầu.) Các gốc thứ cấp (ở giữa chuỗi) ổn định hơn các gốc chính (ở cuối chuỗi gốc) chuỗi) và các gốc cấp ba (tại một điểm nhánh) ổn định hơn. Mỗi khi một monome ethylene được thêm vào, nó sẽ tạo ra một gốc chính, nhưng thường những thứ này sẽ sắp xếp lại để tạo thành các gốc thứ cấp hoặc bậc ba ổn định hơn. Việc bổ sung các monome ethylene vào các vị trí thứ cấp hoặc đại học tạo ra sự phân nhánh.
Polyetylen mật độ rất thấp (VLDPE) [ chỉnh sửa ]
VLDPE được xác định bởi phạm vi mật độ 0,880, 0,915 g / cm 3 . VLDPE là một loại polymer tuyến tính đáng kể với mức độ cao của các chuỗi chuỗi ngắn, thường được tạo ra bằng cách đồng trùng hợp ethylene với các alpha-olefin chuỗi ngắn (ví dụ, 1-butene, 1-hexene và 1-octene). VLDPE được sản xuất phổ biến nhất bằng cách sử dụng các chất xúc tác luyện kim do sự kết hợp đồng phân lớn hơn được thể hiện bởi các chất xúc tác này. VLDPE được sử dụng cho vòi và ống, túi thực phẩm đông lạnh và đá, bao bì thực phẩm và bọc căng cũng như bộ điều chỉnh tác động khi pha trộn với các polyme khác.
Gần đây, nhiều hoạt động nghiên cứu đã tập trung vào bản chất và phân phối các nhánh chuỗi dài bằng polyetylen. Trong HDPE, một số lượng tương đối nhỏ của các nhánh này, có thể là một trong 100 hoặc 1.000 nhánh trên mỗi carbon xương sống, có thể ảnh hưởng đáng kể đến tính chất lưu biến của polymer.
Các chất đồng trùng hợp [ chỉnh sửa ]
Ngoài việc đồng trùng hợp với alpha-olefin, ethylene cũng có thể là chất đồng trùng hợp với nhiều loại monome và ion khác tạo ra gốc tự do. Các ví dụ phổ biến bao gồm vinyl acetate (sản phẩm tạo ra là copolyme ethylene-vinyl acetate, hoặc EVA, được sử dụng rộng rãi trong bọt đế giày thể thao) và nhiều loại acrylate. Các ứng dụng của copolyme acrylic bao gồm bao bì và đồ thể thao, và phụ gia siêu dẻo, được sử dụng để sản xuất xi măng.
Cấu trúc phân tử của các loại PE khác nhau [ chỉnh sửa ]
Hành vi vật liệu đa dạng của các loại polyetylen khác nhau có thể được giải thích bằng cấu trúc phân tử của chúng. Trọng lượng phân tử và độ kết tinh đang có tác động lớn nhất, sự kết tinh lần lượt phụ thuộc vào trọng lượng phân tử và mức độ phân nhánh. Chuỗi polymer càng ít phân nhánh và trọng lượng phân tử càng nhỏ thì độ kết tinh của polyetylen càng cao. Độ kết tinh nằm trong khoảng từ 35% (PE-LD / PE-LLD) đến 80% (PE-HD). Trong tinh thể polyetylen có mật độ 1,0 g · cm 3 trong các vùng vô định hình 0,86 g · cm 3 . Do đó, một mối quan hệ gần như tuyến tính tồn tại giữa mật độ và độ kết tinh. [13]
Mức độ phân nhánh của các loại polyetylen khác nhau có thể được biểu diễn dưới dạng sơ đồ như sau: [13]
Hình vẽ cho thấy xương sống bằng polyetylen, nhánh chuỗi ngắn và nhánh chuỗi bên. Các chuỗi polymer được biểu diễn một cách tuyến tính.
Các nhánh chuỗi [ chỉnh sửa ]
Các tính chất của polyetylen phụ thuộc nhiều vào loại và số nhánh của chuỗi. Các nhánh chuỗi lần lượt phụ thuộc vào quá trình được sử dụng: hoặc là quá trình áp suất cao (chỉ PE-LD) hoặc quá trình áp suất thấp (tất cả các loại PE khác). Polyetylen mật độ thấp được sản xuất bởi quá trình áp suất cao bằng cách trùng hợp gốc, do đó nhiều nhánh chuỗi ngắn cũng như nhánh chuỗi dài được hình thành. Các nhánh chuỗi ngắn được hình thành bởi các phản ứng chuyển chuỗi nội phân tử, chúng luôn là các nhánh chuỗi butyl hoặc ethyl vì phản ứng tiến hành sau cơ chế sau:
Các vấn đề môi trường [ chỉnh sửa ]
|
Phần này cần mở rộng . Bạn có thể giúp đỡ bằng cách thêm vào nó. ( Tháng 8 năm 2018 )
|

Polyetylen được sản xuất từ ethylene, và mặc dù ethylene có thể được sản xuất từ tái chế tài nguyên, nó chủ yếu được lấy từ dầu mỏ hoặc khí đốt tự nhiên.
Hơn nữa, việc sử dụng rộng rãi polyetylen gây khó khăn cho việc quản lý chất thải nếu nó không được tái chế. Polyetylen không dễ phân hủy sinh học, và do đó tích lũy trong các bãi chôn lấp. Thiêu đốt có thể dẫn đến phát thải khí độc hại.
Tại Nhật Bản, loại bỏ nhựa theo cách thân thiện với môi trường là vấn đề chính được thảo luận cho đến khi thảm họa Fukushima năm 2011 trở thành một vấn đề lớn hơn. Nó được liệt kê là một thị trường trị giá 90 tỷ đô la cho các giải pháp. Kể từ năm 2008, Nhật Bản đã nhanh chóng tăng cường tái chế nhựa, nhưng vẫn còn một lượng lớn bao bì nhựa bị lãng phí. [22]
Năm 2010, một nhà nghiên cứu người Nhật, Akinori Ito, đã phát hành nguyên mẫu của một cỗ máy tạo ra dầu từ polyetylen bằng cách sử dụng quy trình chưng cất hơi nhỏ, khép kín. [23]
Khả năng phân hủy sinh học [ chỉnh sửa ]
Polyetylen không dễ dàng phân hủy trong các bãi chôn lấp . Tuy nhiên, có một số loài vi khuẩn và động vật có khả năng làm suy giảm polyetylen.
Vào tháng 5 năm 2008, Daniel Burd, một người Canada 16 tuổi, đã giành được Hội chợ Khoa học toàn Canada tại Ottawa sau khi phát hiện ra rằng Pseudomonas fluorescens với sự giúp đỡ của Sp Breathomonas , có thể làm giảm hơn 40% trọng lượng của túi nhựa trong vòng chưa đầy ba tháng. [24]
Vi khuẩn ưa nhiệt Brevibacillus borstelensis (chủng 707) được phân lập từ đất mẫu và được tìm thấy để sử dụng polyetylen mật độ thấp làm nguồn carbon duy nhất khi được ủ với nhau ở 50 ° C. Phân hủy sinh học tăng theo thời gian tiếp xúc với bức xạ cực tím. [25]
Acinetobacter sp. 351 có thể làm suy giảm các oligome PE có trọng lượng phân tử thấp hơn. Khi PE chịu tác dụng oxy hóa nhiệt và quang hóa, các sản phẩm bao gồm ankan, anken, xeton, aldehyd, rượu, axit cacboxylic, axit keto, axit dicarboxylic, lacton và este được phát hành.
Vào năm 2014, một nhà nghiên cứu Trung Quốc đã phát hiện ra rằng ấu trùng bột ăn Ấn Độ có thể chuyển hóa polyetylen từ việc quan sát rằng túi nhựa ở nhà anh ta có những lỗ nhỏ. Do suy nghĩ rằng ấu trùng đói phải tiêu hóa nhựa bằng cách nào đó, anh và nhóm của mình đã phân tích vi khuẩn đường ruột của chúng và tìm thấy một số ít có thể sử dụng nhựa làm nguồn carbon duy nhất của chúng. Không chỉ các vi khuẩn từ ruột của Plodia interpuncella ấu trùng bướm có thể chuyển hóa polyetylen, chúng làm suy giảm đáng kể, giảm độ bền kéo của nó xuống 50%, khối lượng của nó xuống 10% và trọng lượng phân tử của chuỗi polyme của nó 13%. [27] [28]
Năm 2017, các nhà nghiên cứu đã báo cáo rằng sâu bướm của Galleria mellonella ăn rác nhựa như polyetylen. ] Biến đổi khí hậu [ chỉnh sửa ]
Khi tiếp xúc với bức xạ mặt trời xung quanh, nhựa tạo ra hai khí nhà kính là metan và ethylene. Quan tâm đặc biệt là loại nhựa giải phóng khí ở tốc độ cao nhất: polyetylen mật độ thấp (hoặc LDPE). Do tính chất mật độ thấp, nó bị phá vỡ dễ dàng hơn theo thời gian, dẫn đến diện tích bề mặt cao hơn. Việc sản xuất các loại khí vi lượng này từ LDPE nguyên chất tăng theo diện tích / thời gian bề mặt, với tốc độ ở giai đoạn ủ trong vòng 212 ngày là 5,8nmol g-1 d-1 của metan, 14,5nmol g-1 d-1 của ethylene, 3,9nmol g-1 d-1 ethane và 9,7nmol g-1 d-1 propylene. Khi được ủ trong không khí, LDPE phát ra các chất khí với tốc độ ~ 2 lần và ~ 76 lần so với nước đối với metan và ethylene, tương ứng. [31]
Polyethylen biến đổi hóa học [ chỉnh sửa ]
Polyetylen có thể được biến đổi trong phản ứng trùng hợp bởi các nhà phân tích cực hoặc không phân cực hoặc sau khi trùng hợp thông qua các phản ứng tương tự polymer. Các phản ứng tương tự polymer phổ biến là trong trường hợp liên kết ngang polyetylen, clo hóa và sulfochlor hóa.
Các chất đồng trùng hợp etylen không phân cực [ chỉnh sửa ]
α-olefin [ chỉnh sửa ]
Trong quá trình áp suất thấp ví dụ 1-butene hoặc 1-hexene) có thể được thêm vào, được kết hợp trong chuỗi polymer trong quá trình trùng hợp. Các copolyme này giới thiệu chuỗi bên ngắn, do đó độ kết tinh và mật độ giảm. Như đã giải thích ở trên, tính chất cơ học và nhiệt được thay đổi qua đó. Đặc biệt, PE-LLD được sản xuất theo cách này.
Polyethylen polyetylen (PE-MC) [ chỉnh sửa ]
Polyetylen (PE-M) được điều chế bằng các chất xúc tác luyện kim, thường bao gồm các chất đồng trùng hợp (z. B. ethene / hexene). Metallocene polyetylen có phân bố trọng lượng phân tử tương đối hẹp, độ bền đặc biệt cao, tính chất quang học tuyệt vời và hàm lượng comonomer thống nhất. Do sự phân bố trọng lượng phân tử hẹp, nó hoạt động ít giả hơn (đặc biệt là dưới tốc độ cắt lớn hơn). Metallocene polyetylen có tỷ lệ thấp các thành phần trọng lượng phân tử thấp (có thể chiết xuất) và nhiệt độ hàn và hàn thấp. Do đó, nó đặc biệt phù hợp với ngành công nghiệp thực phẩm. [13]: 238 [32]: 19
Polyetylen với phân bố trọng lượng phân tử đa phương thức [ chỉnh sửa ] Polyetylen với phân bố trọng lượng phân tử đa phương thức bao gồm một số phân đoạn polymer, được trộn đồng nhất. Các loại polyetylen như vậy cung cấp độ cứng cực cao, độ dẻo dai, sức mạnh, khả năng chống nứt ứng suất và tăng khả năng chống lan truyền vết nứt. Chúng bao gồm các tỷ lệ bằng nhau phân số polymer cao hơn và thấp hơn. Các đơn vị trọng lượng phân tử thấp kết tinh dễ dàng hơn và thư giãn nhanh hơn. Các phân số trọng lượng phân tử cao hơn hình thành liên kết các phân tử giữa các tinh thể, do đó làm tăng độ bền và khả năng chống nứt ứng suất. Polyetylen với phân bố trọng lượng phân tử đa phương thức có thể được điều chế trong các lò phản ứng hai giai đoạn, bằng các chất xúc tác với hai trung tâm hoạt động khác nhau trên một chất mang hoặc bằng cách trộn trong các máy đùn. [13]: 238
copolyme olefin (COC) 19659007] [ chỉnh sửa ]
Các chất đồng trùng hợp olefin tuần hoàn được điều chế bằng cách đồng trùng hợp ethene và cycloolefin (thường là norbornene) được sản xuất bằng cách sử dụng chất xúc tác metallicoxene. Các polyme thu được là các polime vô định hình và đặc biệt trong suốt và chịu nhiệt. [13]: 239 [32]: 27
Các chất đồng trùng hợp ethylene cực []
Các hợp chất cơ bản được sử dụng làm chất khử cực là rượu vinyl (Ethenol, một loại rượu không bão hòa), axit acrylic (axit propenoic, một axit không bão hòa) và các este có chứa một trong hai hợp chất.
Các chất đồng trùng hợp etylen với rượu không bão hòa [ chỉnh sửa ]
Chất đồng trùng hợp etylen / vinyl rượu (EVOH) là (chính thức) là một chất đồng trùng hợp của PE và rượu vinyl (ethenol). (một phần) thủy phân copolyme ethylene-vinyl acetate (vì bản thân rượu vinyl không ổn định). Tuy nhiên, thông thường EVOH có hàm lượng comonomer cao hơn VAC thường được sử dụng. [33]: 239
EVOH được sử dụng trong màng nhiều lớp để đóng gói dưới dạng lớp rào cản (nhựa chắn). Vì EVOH hút ẩm (thu hút nước), nó hấp thụ nước từ môi trường, do đó nó mất tác dụng rào cản. Do đó, nó phải được sử dụng làm lớp lõi được bao quanh bởi các loại nhựa khác (như LDPE, PP, PA hoặc PET). EVOH cũng được sử dụng làm chất phủ chống ăn mòn ở đèn đường, cột đèn giao thông và tường chống ồn. [33]: 239
copolyme axit ethylene / acrylic (EAA) [ chỉnh sửa ]
Copolyme của etylen và axit cacboxylic không bão hòa (như axit acrylic) được đặc trưng bởi độ bám dính tốt với các vật liệu khác nhau, bởi khả năng chống nứt ứng suất và tính linh hoạt cao. [34] Tuy nhiên, chúng nhạy cảm hơn với nhiệt và oxy hóa. hơn đồng phân ethylene. Các chất đồng trùng hợp etylen / axit acrylic được sử dụng làm chất kích thích bám dính. [13]
Nếu muối của axit cacboxylic không bão hòa có trong polyme, mạng ion ion thuận nghịch được hình thành, chúng được gọi là ionomer. Ionomer là nhựa nhiệt dẻo có độ trong suốt cao, được đặc trưng bởi độ bám dính cao với kim loại, khả năng chịu mài mòn cao và độ hấp thụ nước cao. [13]
Chất đồng trùng hợp etylen với este không bão hòa [ chỉnh sửa ]
với ethylene, hoặc nửa cồn có thể nằm trong xương sống polymer (như trường hợp của copolyme ethylene-vinyl acetate) hoặc của moọc axit (ví dụ như trong copolyme ethylene-ethyl acrylate). Copolyme ethylene-vinyl acetate được điều chế tương tự LD-PE bằng cách trùng hợp áp suất cao. Tỷ lệ của comonomer có ảnh hưởng quyết định đến hành vi của polymer.
Mật độ giảm tới 10% tỷ lệ của nhà phân tích vì sự hình thành tinh thể bị xáo trộn. Với tỷ lệ cao hơn, nó tiếp cận với một trong các polyvinyl axetat (1,17 g / cm 3 ). [33]: 235 Do chất đồng trùng hợp etylen vinyl axetat tinh thể giảm dần. Nội dung. Các nhóm bên cực thay đổi đáng kể tính chất hóa học (so với polyetylen): [13]: 224 khả năng chống chịu thời tiết, độ bám dính và khả năng hàn tăng với hàm lượng comonomer, trong khi độ kháng hóa học giảm. Ngoài ra các tính chất cơ học cũng được thay đổi: khả năng chống nứt ứng suất và độ bền khi tăng lạnh, trong khi đó ứng suất và ứng suất nhiệt giảm. Với tỷ lệ rất cao của các nhà phân tích (khoảng 50%) nhựa nhiệt dẻo cao su được sản xuất (chất đàn hồi nhiệt dẻo). [33]: 235
Chất đồng trùng hợp etylen-etyl acryat copolyme. [13]: 240
Liên kết ngang [ chỉnh sửa ]
Một sự phân biệt cơ bản được tạo ra giữa liên kết ngang peroxide (PE-Xa), liên kết ngang silic (PE-Xa) , liên kết ngang chùm electron (PE-Xc) và liên kết ngang azo (PE-Xd). [35]
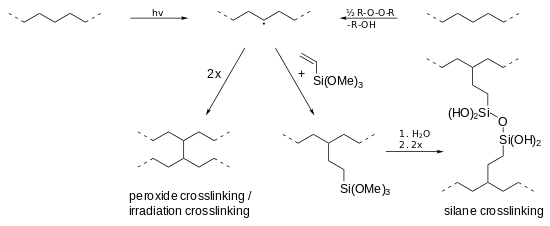
Hiển thị là peroxide, liên kết ngang silane và chiếu xạ. Trong mỗi phương pháp, một gốc được tạo ra trong chuỗi polyetylen (trung tâm trên cùng), bằng bức xạ (h · ν) hoặc bằng peroxit (R-O-O-R). Then, two radical chains can either directly crosslink (bottom left) or indirectly by silane compounds (bottom right).
- Peroxide crosslinking (PE-Xa): The crosslinking of polyethylene using peroxides (e. g. dicumyl or di-tert-butyl peroxide) is still of major importance. In the so-called Engel processa mixture of HDPE and 2 %[36] peroxide is at first mixed at low temperatures in an extruder and then crosslinked at high temperatures (between 200 and 250 °C).[35] The peroxide decomposes to peroxide radicals (RO•), which abstract (remove) hydrogen atoms from the polymer chain, leading to radicals. When these combine, a crosslinked network is formed.[37] The resulting polymer network is uniform, of low tension and high flexibility, whereby it is softer and tougher than (the irradiated) PE-Xc.[35]
- Silane crosslinking (PE-Xb): In the presence of silanes (e.g. trimethoxyvinylsilane) polyethylene can initially be Si-functionalized by irradiation or by a small amount of a peroxide. Later Si-OH groups can be formed in a water bath by hydrolysis, which condense then and crosslink the PE by the formation of Si-O-Si bridges. [16] Catalysts such as dibutyltin dilaurate may accelerate the reaction.[36]
- Irradiation crosslinking (PE-Xc): The crosslinking of polyethylene is also possible by a downstream radiation source (usually an electron accelerator, occasionally a isotopic radiator). PE products are crosslinked below the crystalline melting point by splitting off hydrogen atoms. β-radiation possesses a penetration depth of 10 mm, ɣ-radiation 100 mm. Thereby the interior or specific areas can be excluded from the crosslinking.[35] However, due to high capital and operating costs radiation crosslinking plays only a minor role compared with the peroxide crosslinking.[33] In contrast to peroxide crosslinking, the process is carried out in the solid state. Thereby, the cross-linking takes place primarily in the amorphous regions, while the crystallinity remains largely intact.[36]
- Azo crosslinking (PE-Xd): In the so-called Lubonyl process polyethylene is crosslinked preadded azo compounds after extrusion in a hot salt bath.[33][35]
Chlorination and sulfochlorination[edit]
Chlorinated Polyethylene (PE-C) is an inexpensive material having a chlorine content from 34 to 44%. It is used in blends with PVC because the soft, rubbery chloropolyethylene is embedded in the PVC matrix, thereby increasing the impact resistance. In addition, it also increases the weather resistance. Furthermore, it is used for softening PVC foils, without risking the migrate of plasticizers. Chlorinated polyethylene can be crosslinked peroxidically to form an elastomer which is used in cable and rubber industry.[33] When chlorinated polyethylene is added to other polyolefins, it reduces the flammability.[13]:245
Chlorosulfonated PE (CSM) is used as starting material for ozone resistant synthetic rubber.[38]
Bio-based polyethylene[edit]
Braskem and Toyota Tsusho Corporation started joint marketing activities to produce polyethylene from sugarcane. Braskem will build a new facility at their existing industrial unit in Triunfo, Rio Grande do Sul, Brazil with an annual production capacity of 200,000 short tons (180,000,000 kg), and will produce high-density and low-density polyethylene from bioethanol derived from sugarcane.[39]
Polyethylene can also be made from other feedstocks, including wheat grain and sugar beet. These developments are using renewable resources rather than fossil fuel, although the issue of plastic source is currently negligible in the wake of plastic waste and in particular polyethylene waste as shown above.
Nomenclature and general description of the process[edit]
The name polyethylene comes from the ingredient and not the resulting chemical compound, which contains no double bonds. The scientific name polyethene is systematically derived from the scientific name of the monomer.[40][41] The alkene monomer converts to a long, sometimes very long, alkane in the polymerization process.[41] In certain circumstances it is useful to use a structure-based nomenclature; in such cases IUPAC recommends poly(methylene) (poly(methanediyl) is a non-preferred alternative).[40] The difference in names between the two systems is due to the opening up of the monomer's double bond upon polymerization.[42] The name is abbreviated to PE. In a similar manner polypropylene and polystyrene are shortened to PP and PS, respectively. In the United Kingdom and India the polymer is commonly called polythenefrom the ICI trade name, although this is not recognized scientifically.
References[edit]
- ^ Compendium of Polymer Terminology and Nomenclature – IUPAC Recommendations 2008 (pdf). Retrieved 2018-08-28.
- ^ a b Batra, Kamal (2014). Role of Additives in Linear Low Density Polyethylene (LLDPE) Films. tr. 9. Retrieved 16 September 2014.
- ^ "poly(ethylene)_msds".
- ^ Wapler, M. C.; Leupold, J.; Dragonu, I.; von Elverfeldt, D.; Zaitsev, M.; Wallrabe, U. (2014). "Magnetic properties of materials for MR engineering, micro-MR and beyond". JMR. 242: 233–242. arXiv:1403.4760. Bibcode:2014JMagR.242..233W. doi:10.1016/j.jmr.2014.02.005. PMID 24705364.
- ^ Geyer, Roland; Jambeck, Jenna R.; Law, Kara Lavender (2017-07-01). "Production, use, and fate of all plastics ever made". Science Advances. 3 (7): e1700782. Bibcode:2017SciA….3E0782G. doi:10.1126/sciadv.1700782. PMC 5517107. PMID 28776036.
- ^ "Plastics: The Facts" (PDF). Plastics Europe. Retrieved 2018-08-29.
- ^ von Pechmann, H. (1898). "Ueber Diazomethan und Nitrosoacylamine". Berichte der Deutschen Chemischen Gesellschaft zu Berlin. 31: 2640–2646.
page 2643: Erwähnt sei noch, dass aus einer ätherischen Diazomethanlösung sich beim Stehen manchmal minimale Quantitäten eines weissen, flockigen, aus Chloroform krystallisirenden Körpers abscheiden; … (It should be mentioned that from an ether solution of diazomethane, upon standing, sometimes small quantities of a white, flakey substance, which can be crystallized from chloroform, precipitate; … )
- ^ Bamberger claimed that one of his students, Hindermann, had noted the formation of polyethylene in 1897. Eug. Bamberger & Fred. Tschirner (1900) "Ueber die Einwirkung von Diazomethan auf β-Arylhydroxylamine" (On the effect of diazomethane on β-arylhydroxylamine), Berichte der Deutschen chemischen Gesellschaft zu Berlin33: 955–959. From footnote 3 on page 956: "Die Abscheidung weisser Flocken aus Diazomethanlösungen erwähnt auch v. Pechmann (diese Berichte 31, 2643); er hat sie aber wegen Substanzmangel nicht untersucht. Ich hatte übrigens Hrn. v. Pechmann schon einige Zeit vor Erscheinen seiner Publication mitgetheilt, dass aus Diazomethan ein fester, weisser Körper entstehe, der sich bei der Analyse als (CH2)x erwiesen habe, worauf mir Hr. v. Pechmann schrieb, dass er den weissen Körper ebensfalls beobachtet, aber nicht untersucht habe. Zuerst erwähnt ist derselbe in der Dissertation meines Schülers Hindermann, Zürich (1897), S. 120." (Von Pechmann (these Reports312643) also mentioned the precipitation of white flakes from diazomethane solutions; however, due to a scarcity of the material, he didn't investigate it. Incidentally, some time before the appearance of his publication, I had communicated to Mr. von Pechmann that a solid, white substance arose from diazomethane, which on analysis proved to be (CH2)xwhereupon Mr. von Pechmann wrote me that he had likewise observed the white substance, but not investigated it. It is first mentioned in the dissertation of my student Hindermann, Zürich (1897), p. 120.)
- ^ Eug. Bamberger & Fred. Tschirner (1900) "Ueber die Einwirkung von Diazomethan auf β-Arylhydroxylamine" (On the effect of diazomethane on β-arylhydroxylamine), Berichte der Deutschen chemischen Gesellschaft zu Berlin33: 955–959. From page 956: "Eine theilweise — übrigens immer nur minimale — Umwandlung des Diazomethans in Stickstoff und Polymethylen vollzieht sich auch bei ganz andersartigen Reactionen; … " (A partial — incidentally, always only minimal — conversion of diazomethane into nitrogen and polymethylene takes place also during quite different reactions; … )
- ^ "Winnington history in the making". This is Cheshire. 23 August 2006. Archived from the original on 21 January 2010. Retrieved 20 February 2014.
- ^ "Poly – The All Star Plastic". Popular Mechanics. 91 (1). July 1949. pp. 125–129. Retrieved 20 February 2014.
- ^ Hoff, Ray; Mathers, Robert T. (2010). "Chapter 10. Review of Phillips Chromium Catalyst for Ethylene Polymerization". In Hoff, Ray; Mathers, Robert T. Handbook of Transition Metal Polymerization Catalysts. John Wiley & Sons. doi:10.1002/9780470504437.ch10. ISBN 978-0-470-13798-7.
- ^ a b c d e f g h i j k Kaiser, Wolfgang (2011). Kunststoffchemie für Ingenieure von der Synthese bis zur Anwendung (3. ed.). München: Hanser. ISBN 978-3-446-43047-1.
- ^ a b c Whiteley, Kenneth S.; Heggs, T. Geoffrey; Koch, Hartmut; Mawer, Ralph L. and Immel, Wolfgang (2005) "Polyolefins" in Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH, Weinheim. doi:10.1002/14356007.a21_487
- ^ "How to Identify Plastic Materials Using The Burn Test". Boedeker Plastics. Retrieved 8 May 2012.
- ^ Chung, C. I. (2010) Extrusion of Polymers: Theory and Practice. 2nd ed.. Hanser: Munich.
- ^ a b Plastics Design Library (1997). Handbook of Plastics Joining: A Practical Guide. Norwich, New York: Plastics Design Library. tr. 326. ISBN 1-884207-17-0.
- ^ Kurtz, Steven M. (2015). UHMWPE Biomaterials Handbook. Ultra-High Molecular Weight Polyethylene in Total Joint Replacement and Medical Devices (3rd ed.). Yêu tinh khác. tr. 3. doi:10.1016/C2013-0-16083-7. ISBN 9780323354356.
- ^ "Market Study: Polyethylene – HDPE". Ceresana Research. May 2012. Retrieved 8 May 2012.
- ^ "Market Study: Polyethylene – LLDPE 2nd. edition". Ceresana. November 2014. Retrieved 3 February 2015.
- ^ "Market Study: Polyethylene – LDPE (2nd edition)". Ceresana. October 2014. Retrieved 3 February 2015.
- ^ Prideaux, Eric (3 November 2007). "Plastic incineration rise draws ire". Japan Times. Archived from the original on 22 November 2012. Retrieved 8 May 2012.
- ^ Nguyen, Tuan (17 February 2011). "New invention turns plastic bags into oil". smartplanet.com. Retrieved 20 February 2014.
- ^ "CanadaWorld – WCI student isolates microbe that lunches on plastic bags". The Record.com. Archived from the original on 18 July 2011. Retrieved 20 February 2014.
- ^ Hadad, D.; Geresh, S.; Sivan, A. (2005). "Biodegradation of polyethylene by the thermophilic bacterium Brevibacillus borstelensis". Journal of Applied Microbiology. 98 (5): 1093–1100. doi:10.1111/j.1365-2672.2005.02553.x. PMID 15836478.
- ^ Tokiwa, Yutaka; Calabia, Buenaventurada P.; Ugwu, Charles U.; Aiba, Seiichi (September 2009). "Biodegradability of Plastics". International Journal of Molecular Sciences. 10 (9): 3722–3742. doi:10.3390/ijms10093722. PMC 2769161. PMID 19865515.
- ^ Balster, Lori (27 January 2015). "Discovery of plastic-eating bacteria may speed waste reduction". fondriest.com.
- ^ Yang, Jun; Yang, Yu; Wu, Wei-Min; Zhao, Jiao; Jiang, Lei (2014). "Evidence of Polyethylene Biodegradation by Bacterial Strains from the Guts of Plastic-Eating Waxworms". Environmental Science & Technology. 48 (23): 13776–84. Bibcode:2014EnST…4813776Y. doi:10.1021/es504038a. PMID 25384056.
- ^ "Forscherin entdeckt zufällig Plastik-fressende Raupe" (in German). Der Spiegel. April 24, 2017. Retrieved April 24, 2017.
- ^ Briggs, Helen. "Plastic-eating caterpillar could munch waste, scientists say". BBC News. Retrieved 24 April 2017.
- ^ Karl, David M.; Wilson, Samuel T.; Ferrón, Sara; Royer, Sarah-Jeanne (1 August 2018). "Production of methane and ethylene from plastic in the environment". XIN MỘT . 13 (8): e0200574. doi:10.1371/journal.pone.0200574. ISSN 1932-6203.
- ^ a b Pascu, Cornelia Vasile: Mihaela (2005). Practical guide to polyethylene ([Online-Ausg.]. ed.). Shawbury: Rapra Technology Ltd. ISBN 978-1859574935.
- ^ a b c d e f g Elsner, Peter; Eyerer, Peter; Hirth, Thomas (2012). Domininghaus – Kunststoffe (8. ed.). Berlin Heidelberg: Springer-Verlag. tr. 224. ISBN 978-3-642-16173-5.
- ^ Elsner, Peter; Eyerer, Peter and Hirth, Thomas (2012). Kunststoffe Eigenschaften und Anwendungen (8. ed.). Berlin, Heidelberg: Springer Berlin Heidelberg. ISBN 978-3-642-16173-5.CS1 maint: Multiple names: authors list (link)
- ^ a b c d e Baur, Erwin; Osswald, Tim A. (October 2013). Saechtling Kunststoff Taschenbuch. tr. 443. ISBN 978-3-446-43729-6.Vorschau auf kunststoffe.de
- ^ a b c Whiteley, Kenneth S. (2011). Polyethylene. Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a21_487.pub2. ISBN 978-3527306732.
- ^ Koltzenburg, Sebastian; Maskos, Michael; Nuyken, Oskar (2014). Polymere: Synthese, Eigenschaften und Anwendungen (1 ed.). Springer Spektrum. tr. 406. ISBN 978-3-642-34773-3.
- ^ Chlorsulfoniertes Polyethylen (CSM). ChemgaPedia.de
- ^ "Braskem & Toyota Tsusho start joint marketing activities for green polyethylene from sugar cane" (Press release). yourindustrynews.com. 26 September 2008. Retrieved 20 February 2014.
- ^ a b A Guide to IUPAC Nomenclature of Organic Compounds (Recommendations 1993) IUPAC, Commission on Nomenclature of Organic Chemistry. Blackwell Scientific Publications. 1993. ISBN 978-0632037025. Retrieved 20 February 2014.
- ^ a b Kahovec, J.; Fox, R. B.; Hatada, K. (2002). "Nomenclature of regular single-strand organic polymers (IUPAC Recommendations 2002)". Pure and Applied Chemistry. 74 (10): 1921. doi:10.1351/pac200274101921.
- ^ "IUPAC Provisional Recommendations on the Nomenclature of Organic Chemistry". International Union of Pure and Applied Chemistry. 27 October 2004. Retrieved 20 February 2014.
Bibliography[edit]
External links[edit]
