Lanthan – Wikipedia
chemisches Element mit der Ordnungszahl 57
Chemisches Element mit der Ordnungszahl 57
 |
|||||||||||||||
| Lanthan | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Aussprache | |
||||||||||||||
| Aussehen | Silbrig Weiß | ||||||||||||||
| Standardatomgewicht EINr, std(La) | 138.90547(7)[1] | ||||||||||||||
| Lanthan im Periodensystem | |||||||||||||||
| Ordnungszahl ((Z.) | 57 | ||||||||||||||
| Gruppe | Gruppe 3 (manchmal als Gruppe n / a angesehen) | ||||||||||||||
| Zeitraum | Zeitraum 6 | ||||||||||||||
| Block | D-Block (manchmal als F-Block betrachtet) | ||||||||||||||
| Elementkategorie | Lanthanid, manchmal als Übergangsmetall angesehen | ||||||||||||||
| Elektronenkonfiguration | [Xe] 5d1 6s2 | ||||||||||||||
| Elektronen pro Schale | 2, 8, 18, 18, 9, 2 | ||||||||||||||
| Physikalische Eigenschaften | |||||||||||||||
| Phase beim STP | solide | ||||||||||||||
| Schmelzpunkt | 1193 K (920 ° C, 1688 ° F) | ||||||||||||||
| Siedepunkt | 3737 K (3464 ° C, 6267 ° F) | ||||||||||||||
| Dichte (nahe rt) | 6,162 g / cm3 | ||||||||||||||
| wenn flüssig (bei mp) | 5,94 g / cm3 | ||||||||||||||
| Schmelzwärme | 6,20 kJ / mol | ||||||||||||||
| Verdampfungswärme | 400 kJ / mol | ||||||||||||||
| Molare Wärmekapazität | 27,11 J / (mol · K) | ||||||||||||||
Dampfdruck (extrapoliert)
|
|||||||||||||||
| Atomeigenschaften | |||||||||||||||
| Oxidationszustände | 0,[2] +1, +2, +3 (ein stark basisches Oxid) | ||||||||||||||
| Elektronegativität | Pauling-Skala: 1.10 | ||||||||||||||
| Ionisierungsenergien |
|
||||||||||||||
| Atomradius | empirisch: 187 Uhr | ||||||||||||||
| Kovalenter Radius | 207 ± 20 Uhr | ||||||||||||||
|
Spektrallinien von Lanthan |
|||||||||||||||
| Andere Eigenschaften | |||||||||||||||
| Natürliches Vorkommen | ursprünglich | ||||||||||||||
| Kristallstruktur | Doppelt hexagonal dicht gepackt (dhcp)
 |
||||||||||||||
| Schallgeschwindigkeit dünner Stab | 2475 m / s (bei 20 ° C) | ||||||||||||||
| Wärmeausdehnung | α, Poly: 12,1 um / (m · K) (at rt) | ||||||||||||||
| Wärmeleitfähigkeit | 13,4 W / (m · K) | ||||||||||||||
| Elektrischer widerstand | α, Poly: 615 nΩ · m (at rt) | ||||||||||||||
| Magnetische Bestellung | paramagnetisch[3] | ||||||||||||||
| Magnetische Suszeptibilität | + 118,0 · 10−6 cm3/ mol (298 K)[4] | ||||||||||||||
| Elastizitätsmodul | α-Form: 36,6 GPa | ||||||||||||||
| Schubmodul | α-Form: 14,3 GPa | ||||||||||||||
| Volumenmodul | α-Form: 27,9 GPa | ||||||||||||||
| QUERKONTRAKTIONSZAHL | α-Form: 0,280 | ||||||||||||||
| Mohs Härte | 2.5 | ||||||||||||||
| Vickers-Härte | 360–1750 MPa | ||||||||||||||
| Brinellhärte | 350–400 MPa | ||||||||||||||
| CAS-Nummer | 7439-91-0 | ||||||||||||||
| Geschichte | |||||||||||||||
| Entdeckung | Carl Gustaf Mosander (1838) | ||||||||||||||
| Hauptisotope von Lanthan | |||||||||||||||
Lanthan ist ein chemisches Element mit dem Symbol La und Ordnungszahl 57. Es ist ein weiches, duktiles, silberweißes Metall, das an der Luft langsam anläuft und weich genug ist, um mit einem Messer geschnitten zu werden. Es ist der Namensgeber der Lanthanid-Reihe, einer Gruppe von 15 ähnlichen Elementen zwischen Lanthan und Lutetium im Periodensystem, von denen Lanthan das erste und der Prototyp ist. Es wird manchmal auch als das erste Element der Übergangsmetalle der 6. Periode angesehen, das es in Gruppe 3 einordnet.[5] obwohl stattdessen manchmal Lutetium in diese Position gebracht wird.[6] Lanthan wird traditionell zu den Seltenerdelementen gezählt. Die übliche Oxidationsstufe ist +3. Lanthan spielt beim Menschen keine biologische Rolle, ist jedoch für einige Bakterien essentiell. Es ist für den Menschen nicht besonders toxisch, zeigt jedoch eine gewisse antimikrobielle Aktivität.
Lanthan kommt normalerweise zusammen mit Cer und den anderen Seltenerdelementen vor. Lanthan wurde erstmals 1839 vom schwedischen Chemiker Carl Gustaf Mosander als Verunreinigung in Cernitrat gefunden – daher der Name Lanthanaus dem Altgriechischen λανθάνειν ((Lanthanein), was “versteckt liegen” bedeutet. Obwohl Lanthan als Seltenerdelement eingestuft wird, ist es das 28. am häufigsten vorkommende Element in der Erdkruste, fast dreimal so häufig wie Blei. In Mineralien wie Monazit und Bastnäsit macht Lanthan etwa ein Viertel des Lanthanidgehalts aus.[7] Es wird aus diesen Mineralien durch einen Prozess von solcher Komplexität gewonnen, dass reines Lanthanmetall erst 1923 isoliert wurde.
Lanthanverbindungen finden zahlreiche Anwendungen als Katalysatoren, Additive in Glas, Kohlenstoffbogenlampen für Studioleuchten und Projektoren, Zündelemente in Feuerzeugen und Brennern, Elektronenkathoden, Szintillatoren, Gas-Wolfram-Lichtbogenschweißelektroden und andere Dinge. Lanthancarbonat wird als Phosphatbindemittel bei hohen Phosphatspiegeln im Blut bei Nierenversagen verwendet.
Eigenschaften[edit]
Körperlich[edit]
Lanthan ist das erste Element und der erste Prototyp der Lanthanid-Serie. Im Periodensystem erscheint es rechts vom Erdalkalimetall-Barium und links vom Lanthanoid-Cer. Lanthan wird oft als Element der Gruppe 3 angesehen, zusammen mit Scandium, Yttrium und dem schwereren Congener Actinium von Lanthan.[8] obwohl diese Klassifizierung umstritten ist. Die 57 Elektronen eines Lanthanatoms sind in der Konfiguration angeordnet [Xe]5d16s2mit drei Valenzelektronen außerhalb des Edelgaskerns. Bei chemischen Reaktionen gibt Lanthan diese drei Valenzelektronen aus den 5d- und 6s-Unterschalen fast immer ab, um die Oxidationsstufe +3 zu bilden, wodurch die stabile Konfiguration des vorhergehenden Edelgases Xenon erreicht wird.[9] Einige Lanthan (II) -Verbindungen sind ebenfalls bekannt, aber sie sind viel weniger stabil.[10]
Unter den Lanthaniden ist Lanthan außergewöhnlich, da es keine 4f-Elektronen als einzelnes Gasphasenatom aufweist. Daher ist es im Gegensatz zu den stark paramagnetischen späteren Lanthaniden (mit Ausnahme der letzten beiden, Ytterbium und Lutetium, wo die 4f-Schale vollständig gefüllt ist) nur sehr schwach paramagnetisch.[11] Die 4f-Schale aus Lanthan kann jedoch in chemischen Umgebungen teilweise besetzt sein und an der chemischen Bindung teilnehmen, was ein Grund ist, warum sie manchmal als kein Element der Gruppe 3 angesehen wird.[12] Zum Beispiel hängen die Schmelzpunkte der dreiwertigen Lanthaniden mit dem Ausmaß der Hybridisierung der 6s-, 5d- und 4f-Elektronen zusammen (Abnahme mit zunehmender 4f-Beteiligung).[13] und Lanthan hat den zweitniedrigsten (nach Cer) Schmelzpunkt unter allen Lanthaniden: 920 ° C.[14] Die Lanthaniden werden härter, wenn die Reihe durchlaufen wird: Wie erwartet ist Lanthan ein weiches Metall. Lanthan hat bei Raumtemperatur einen relativ hohen spezifischen Widerstand von 615 nΩm; im Vergleich dazu beträgt der Wert für das gute Leiteraluminium nur 26,50 nΩm.[15][16] Lanthan ist das am wenigsten flüchtige der Lanthaniden.[17] Wie die meisten Lanthaniden hat Lanthan bei Raumtemperatur eine hexagonale Kristallstruktur. Bei 310 ° C verwandelt sich Lanthan in eine flächenzentrierte kubische Struktur und bei 865 ° C in eine körperzentrierte kubische Struktur.[16]
Chemisch[edit]
Wie von periodischen Trends erwartet, hat Lanthan den größten Atomradius der Lanthaniden. Daher ist es das reaktivste unter ihnen, läuft an der Luft ziemlich schnell an, wird nach einigen Stunden vollständig dunkel und kann leicht unter Bildung von Lanthan (III) -oxid, La, verbrennen2Ö3, das fast so basisch ist wie Calciumoxid.[18] Eine zentimetergroße Lanthanprobe korrodiert in einem Jahr vollständig, da ihr Oxid wie Eisenrost abplatzt, anstatt eine schützende Oxidbeschichtung wie Aluminium, Scandium und Yttrium zu bilden.[19] Lanthan reagiert mit den Halogenen bei Raumtemperatur unter Bildung der Trihalogenide und bildet beim Erwärmen binäre Verbindungen mit den Nichtmetallen Stickstoff, Kohlenstoff, Schwefel, Phosphor, Bor, Selen, Silizium und Arsen.[9][10] Lanthan reagiert langsam mit Wasser unter Bildung von Lanthan (III) -hydroxid, La (OH)3.[20] In verdünnter Schwefelsäure bildet Lanthan leicht das aquatisierte tripositive Ion [La(H2O)9]3+: Dies ist in wässriger Lösung seit La3+ hat keine d- oder f-Elektronen.[20] Lanthan ist die stärkste und härteste Basis unter den Seltenerdelementen, was wiederum erwartet wird, dass es das größte von ihnen ist.[21]
Isotope[edit]

Natürlich vorkommendes Lanthan besteht aus zwei Isotopen, dem Stall 139La und das ursprüngliche langlebige Radioisotop 138La. 139La ist mit 99,910% des natürlichen Lanthan bei weitem am häufigsten anzutreffen: Es wird im S-Prozess (langsame Neutroneneinfang, der in Sternen mit niedriger bis mittlerer Masse auftritt) und im r-Prozess (schnelle Neutroneneinfangung) hergestellt. die in Kernkollaps-Supernovae auftritt).[22] Das sehr seltene Isotop 138La ist einer der wenigen ursprünglichen ungeraden Kerne mit einer langen Halbwertszeit von 1,05 × 1011 Jahre. Es ist einer der protonenreichen p-Kerne, die in den s- oder r-Prozessen nicht produziert werden können. 138La, zusammen mit dem noch selteneren 180mTa wird im ν-Prozess hergestellt, bei dem Neutrinos mit stabilen Kernen interagieren.[23] Alle anderen Lanthanisotope sind synthetisch: mit Ausnahme von 137Bei einer Halbwertszeit von etwa 60.000 Jahren haben alle eine Halbwertszeit von weniger als einem Tag und die meisten eine Halbwertszeit von weniger als einer Minute. Die Isotope 139La und 140La kommen als Spaltprodukte von Uran vor.[22]
Verbindungen[edit]
Lanthanoxid ist ein weißer Feststoff, der durch direkte Reaktion seiner Bestandteile hergestellt werden kann. Aufgrund der Größe des La3+ Ion, La2Ö3 nimmt eine hexagonale 7-Koordinatenstruktur an, die sich in die 6-Koordinatenstruktur von Scandiumoxid ändert (Sc2Ö3) und Yttriumoxid (Y.2Ö3) bei hoher Temperatur. Wenn es mit Wasser reagiert, entsteht Lanthanhydroxid: Bei der Reaktion entsteht viel Wärme und es ist ein zischendes Geräusch zu hören. Lanthanhydroxid reagiert mit atmosphärischem Kohlendioxid unter Bildung des basischen Carbonats.[24]
Lanthanfluorid ist wasserunlöslich und kann als qualitativer Test für das Vorhandensein von La verwendet werden3+. Die schwereren Halogenide sind alle sehr lösliche zerfließende Verbindungen. Die wasserfreien Halogenide werden durch direkte Reaktion ihrer Elemente hergestellt, da das Erhitzen der Hydrate eine Hydrolyse verursacht: zum Beispiel das Erhitzen von hydratisiertem LaCl3 produziert LaOCl.[24]
Lanthan reagiert exotherm mit Wasserstoff unter Bildung des Dihydrids LaH2eine schwarze, pyrophore, spröde, leitende Verbindung mit der Calciumfluoridstruktur.[25] Dies ist eine nichtstöchiometrische Verbindung, und eine weitere Absorption von Wasserstoff ist bei gleichzeitigem Verlust der elektrischen Leitfähigkeit bis zum salzähnlicheren LaH möglich3 ist erreicht.[24] Wie LaI2 und LaI, LaH2 ist wahrscheinlich eine Elektridverbindung.[24]
Aufgrund des großen Ionenradius und der großen Elektropositivität von La3+gibt es nicht viel kovalenten Beitrag zu seiner Bindung und daher hat es eine begrenzte Koordinationschemie, wie Yttrium und die anderen Lanthaniden.[26] Lanthanoxalat löst sich in Alkalimetalloxalatlösungen nicht sehr stark und [La(acac)3(H2O)2] zersetzt sich um 500 ° C. Sauerstoff ist das häufigste Donoratom in Lanthan-Komplexen, die meist ionisch sind und häufig hohe Koordinationszahlen über 6: 8 aufweisen. Es ist am charakteristischsten und bildet quadratische antiprismatische und dodekadeltaedrische Strukturen. Diese hochkoordinierten Spezies erreichen unter Verwendung von Chelatliganden wie in La die Koordinationszahl 122(DAMIT4)3·9 STUNDEN2O, haben oft einen geringen Symmetriegrad aufgrund stereochemischer Faktoren.[26]
Die Lanthan-Chemie neigt aufgrund der Elektronenkonfiguration des Elements dazu, keine π-Bindung zu beinhalten. Daher ist seine metallorganische Chemie ziemlich begrenzt. Die am besten charakterisierten Organolanthanverbindungen sind der Cyclopentadienylkomplex La (C.5H.5)3, das durch Umsetzung von wasserfreiem LaCl hergestellt wird3 mit NaC5H.5 in Tetrahydrofuran und seinen methylsubstituierten Derivaten.[27]
Geschichte[edit]

1751 entdeckte der schwedische Mineralogist Axel Fredrik Cronstedt ein schweres Mineral aus der Mine in Bastnäs, später Cerit genannt. Dreißig Jahre später schickte der fünfzehnjährige Vilhelm Hisinger aus der Familie, der die Mine gehört, eine Probe davon an Carl Scheele, der darin keine neuen Elemente fand. 1803, nachdem Hisinger Eisenmeister geworden war, kehrte er mit Jöns Jacob Berzelius zum Mineral zurück und isolierte ein neues Oxid, das sie benannten Ceroxid nach dem Zwergplaneten Ceres, der zwei Jahre zuvor entdeckt worden war.[28] Ceria wurde gleichzeitig von Martin Heinrich Klaproth unabhängig in Deutschland isoliert.[29] Zwischen 1839 und 1843 wurde Ceroxid vom schwedischen Chirurgen und Chemiker Carl Gustaf Mosander, der im selben Haus wie Berzelius lebte, als eine Mischung von Oxiden gezeigt: Er trennte zwei andere Oxide, die er nannte Lanthana und Didymie.[30][31] Er zersetzte eine Cer-Nitrat-Probe teilweise, indem er sie an der Luft röstete und dann das resultierende Oxid mit verdünnter Salpetersäure behandelte.[32] Im selben Jahr entdeckte Axel Erdmann, ebenfalls Student am Karolinska-Institut, Lanthan in einem neuen Mineral von der Insel Låven in einem norwegischen Fjord.
Schließlich erklärte Mosander seine Verzögerung und sagte, dass er ein zweites Element aus Cer extrahiert habe, und dies nannte er Didym. Obwohl er es nicht erkannte, war auch Didym eine Mischung, und 1885 wurde es in Praseodym und Neodym getrennt.
Da sich die Eigenschaften von Lanthan nur geringfügig von denen von Cer unterschieden und zusammen mit ihm in seinen Salzen auftraten, benannte er es vom Altgriechischen λανθάνειν [lanthanein] (zündete. versteckt liegen).[29] Relativ reines Lanthanmetall wurde erstmals 1923 isoliert.[10]
Vorkommen und Produktion[edit]
Lanthan ist das dritthäufigste aller Lanthaniden und macht 39 mg / kg der Erdkruste aus, nach Neodym mit 41,5 mg / kg und Cer mit 66,5 mg / kg. Es ist fast dreimal so häufig wie Blei in der Erdkruste.[33] Obwohl Lanthan zu den sogenannten “Seltenerdmetallen” gehört, ist es nicht selten, aber es wird historisch so genannt, weil es seltener ist als “gewöhnliche Erden” wie Kalk und Magnesia, und historisch waren nur wenige Ablagerungen bekannt . Lanthan wird als Seltenerdmetall angesehen, da der Abbau schwierig, zeitaufwändig und teuer ist.[10] Lanthan ist selten das dominierende Lanthanoid, das in den Mineralien der Seltenen Erden vorkommt, und in ihren chemischen Formeln geht gewöhnlich Cer voraus. Seltene Beispiele für La-dominante Mineralien sind Monazit- (La) und Lanthanit- (La).[34]

Die La3+ Das Ion hat eine ähnliche Größe wie die frühen Lanthaniden der Cer-Gruppe (bis zu Samarium und Europium), die unmittelbar im Periodensystem folgen, und tritt daher tendenziell zusammen mit ihnen in Phosphat-, Silikat- und Carbonatmineralien wie Monazit auf ( M.IIIPO4) und Bastnäsit (M.IIICO3F), wobei sich M auf alle Seltenerdmetalle mit Ausnahme von Scandium und radioaktivem Promethium (hauptsächlich Ce, La und Y) bezieht.[35] Bastnäsit fehlt normalerweise in Thorium und den schweren Lanthaniden, und die Reinigung der leichten Lanthaniden daraus ist weniger aufwendig. Nachdem das Erz zerkleinert und gemahlen wurde, wird es zuerst mit heißer konzentrierter Schwefelsäure behandelt, wobei Kohlendioxid, Fluorwasserstoff und Siliciumtetrafluorid entstehen. Das Produkt wird dann getrocknet und mit Wasser ausgelaugt, wobei die frühen Lanthanoidionen, einschließlich Lanthan, in Lösung bleiben .[36]
Das Verfahren für Monazit, das normalerweise alle Seltenen Erden sowie Thorium enthält, ist komplizierter. Monazit kann aufgrund seiner magnetischen Eigenschaften durch wiederholte elektromagnetische Trennung abgetrennt werden. Nach der Trennung wird es mit heißer konzentrierter Schwefelsäure behandelt, um wasserlösliche Sulfate von Seltenen Erden herzustellen. Die sauren Filtrate werden teilweise mit Natriumhydroxid auf pH 3–4 neutralisiert. Thorium fällt als Hydroxid aus der Lösung aus und wird entfernt. Danach wird die Lösung mit Ammoniumoxalat behandelt, um Seltene Erden in ihre unlöslichen Oxalate umzuwandeln. Die Oxalate werden durch Tempern in Oxide umgewandelt. Die Oxide werden in Salpetersäure gelöst, die eine der Hauptkomponenten, Cer, ausschließt, deren Oxid in HNO unlöslich ist3. Lanthan wird durch Kristallisation als Doppelsalz mit Ammoniumnitrat abgetrennt. Dieses Salz ist relativ weniger löslich als andere Seltenerd-Doppelsalze und verbleibt daher im Rückstand.[10] Beim Umgang mit einigen der enthaltenen Rückstände ist Vorsicht geboten 228Ra, die Tochter von 232Th, das ist ein starker Gamma-Emitter.[36] Lanthan ist relativ leicht zu extrahieren, da es nur ein benachbartes Lanthanoid, Cer, enthält, das entfernt werden kann, indem seine Fähigkeit genutzt wird, zum + 4-Zustand oxidiert zu werden. danach kann Lanthan durch das historische Verfahren der fraktionierten Kristallisation von La (NO3)3· 2NH4NEIN3· 4H2O oder durch Ionenaustauschtechniken, wenn eine höhere Reinheit gewünscht wird.[36]
Lanthanmetall wird aus seinem Oxid erhalten, indem es mit Ammoniumchlorid oder Fluorid und Flusssäure auf 300-400ºC erhitzt wird, um das Chlorid oder Fluorid herzustellen:[10]
- La2Ö3 + 6 NH4Cl → 2 LaCl3 + 6 NH3 + 3 H.2Ö
Darauf folgt die Reduktion mit Alkali- oder Erdalkalimetallen in Vakuum- oder Argonatmosphäre:[10]
- LaCl3 + 3 Li → La + 3 LiCl
Reines Lanthan kann auch durch Elektrolyse einer geschmolzenen Mischung aus wasserfreiem LaCl hergestellt werden3 und NaCl oder KCl bei erhöhten Temperaturen.[10]
Anwendungen[edit]

Die erste historische Anwendung von Lanthan war in Gaslaternenmänteln. Carl Auer von Welsbach verwendete eine Mischung aus Lanthanoxid und Zirkonoxid, die er nannte Actinophor Die ursprünglichen Mäntel gaben ein grünes Licht und waren nicht sehr erfolgreich. Seine erste Firma, die 1887 eine Fabrik in Atzgersdorf gründete, scheiterte 1889.[37]
Moderne Verwendungen von Lanthan umfassen:

- Ein Material, das für anodisches Material von Nickel-Metallhydrid-Batterien verwendet wird, ist La (Ni
3.6Mn
0,4Al
0,3Co.
0,7). Aufgrund der hohen Kosten für die Extraktion der anderen Lanthaniden wird anstelle von reinem Lanthan ein Mischmetall mit mehr als 50% Lanthan verwendet. Die Verbindung ist eine intermetallische Komponente der AB
5 Art.[38][39]NiMH-Batterien sind in vielen in den USA verkauften Modellen des Toyota Prius enthalten. Diese größeren Nickel-Metallhydrid-Batterien benötigen für die Herstellung große Mengen Lanthan. Die 2008 Toyota Prius NiMH Batterie benötigt 10 bis 15 Kilogramm Lanthan. Da die Ingenieure die Technologie zur Steigerung der Kraftstoffeffizienz vorantreiben, könnte pro Fahrzeug die doppelte Menge Lanthan erforderlich sein.[40][41][42] - Wasserstoffschwammlegierungen können Lanthan enthalten. Diese Legierungen können in einem reversiblen Adsorptionsprozess das 400-fache ihres eigenen Wasserstoffgasvolumens speichern. Jedes Mal, wenn sie dies tun, wird Wärmeenergie freigesetzt. Daher haben diese Legierungen Möglichkeiten in Energieeinsparungssystemen.[16][43]
- Mischmetall, eine pyrophore Legierung, die in leichteren Feuersteinen verwendet wird, enthält 25% bis 45% Lanthan.[44]
- Lanthanoxid und das Borid werden in elektronischen Vakuumröhren als Heißkathodenmaterialien mit starkem Elektronenemissionsvermögen verwendet. Kristalle von Labor
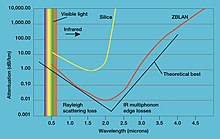
6 werden in thermionischen Elektronenemissionsquellen mit hoher Helligkeit und langer Lebensdauer für Elektronenmikroskope und Hall-Effekt-Triebwerke verwendet.[45] - Lanthan-Trifluorid (LaF
3) ist ein wesentlicher Bestandteil eines schweren Fluoridglases namens ZBLAN. Dieses Glas hat eine überlegene Durchlässigkeit im Infrarotbereich und wird daher für faseroptische Kommunikationssysteme verwendet.[46] - Cer-dotiertes Lanthanbromid und Lanthanchlorid sind die jüngsten anorganischen Szintillatoren, die eine Kombination aus hoher Lichtausbeute, bester Energieauflösung und schneller Reaktion aufweisen. Ihre hohe Ausbeute wandelt sich in eine überlegene Energieauflösung um; Darüber hinaus ist die Lichtleistung über einen sehr weiten Temperaturbereich sehr stabil und recht hoch, was sie für Hochtemperaturanwendungen besonders attraktiv macht. Diese Szintillatoren werden bereits kommerziell häufig in Detektoren von Neutronen oder Gammastrahlen verwendet.[47]
- Carbon-Bogenlampen verwenden eine Mischung aus Seltenerdelementen, um die Lichtqualität zu verbessern. Diese Anwendung, insbesondere von der Filmindustrie für Studiobeleuchtung und -projektion, verbrauchte etwa 25% der Seltenerdverbindungen, die bis zum Ausstieg aus Kohlenstoffbogenlampen hergestellt wurden.[16][48]
- Lanthan (III) oxid (La
2Ö
3) verbessert die Alkalibeständigkeit von Glas und wird aufgrund des hohen Brechungsindex und der geringen Dispersion von Seltenerdgläsern zur Herstellung spezieller optischer Gläser wie Infrarot absorbierendes Glas sowie Kamera- und Teleskoplinsen verwendet.[16] Lanthanoxid wird auch als Kornwachstumsadditiv beim Flüssigphasensintern von Siliziumnitrid und Zirkoniumdiborid verwendet.[49] - Kleine Mengen Lanthan, die Stahl zugesetzt werden, verbessern die Formbarkeit, Schlagfestigkeit und Duktilität, während die Zugabe von Lanthan zu Molybdän die Härte und Empfindlichkeit gegenüber Temperaturschwankungen verringert.[16]
- In vielen Poolprodukten sind geringe Mengen Lanthan enthalten, um die Phosphate zu entfernen, die Algen füttern.[50]
- Lanthanoxid-Additiv zu Wolfram wird in Gas-Wolfram-Lichtbogenschweißelektroden als Ersatz für radioaktives Thorium verwendet.[51][52]
- Verschiedene Verbindungen von Lanthan und anderen Seltenerdelementen (Oxide, Chloride usw.) sind Bestandteile verschiedener Katalysen, wie z. B. Erdölcrackkatalysatoren.[53]
- Die radiometrische Datierung von Lanthan-Barium wird verwendet, um das Alter von Gesteinen und Erzen abzuschätzen, obwohl die Technik nur eine begrenzte Popularität hat.[54]
- Lanthancarbonat wurde als Medikament (Fosrenol, Shire Pharmaceuticals) zur Absorption von überschüssigem Phosphat bei Hyperphosphatämie bei Nierenerkrankungen im Endstadium zugelassen.[55]
- Lanthanfluorid wird in Phosphorlampenbeschichtungen verwendet. Gemischt mit Europiumfluorid wird es auch in der Kristallmembran von ionenselektiven Fluoridelektroden angewendet.[10]
- Wie Meerrettichperoxidase wird Lanthan in der Molekularbiologie als elektronendichter Tracer verwendet.[56]
- Lanthan-modifizierter Bentonit (oder Phoslock) wird verwendet, um Phosphate bei Seebehandlungen aus dem Wasser zu entfernen.[57]
Biologische Rolle[edit]
Lanthan hat beim Menschen keine bekannte biologische Rolle. Das Element wird nach oraler Verabreichung sehr schlecht resorbiert und bei Injektion ist seine Elimination sehr langsam. Lanthancarbonat (Fosrenol) wurde als Phosphatbindemittel zur Absorption von überschüssigem Phosphat bei Nierenerkrankungen im Endstadium zugelassen.[55]
Während Lanthan pharmakologische Wirkungen auf mehrere Rezeptoren und Ionenkanäle hat, ist seine Spezifität für den GABA-Rezeptor unter dreiwertigen Kationen einzigartig. Lanthan wirkt an derselben Modulationsstelle am GABA-Rezeptor wie Zink, ein bekannter negativer allosterischer Modulator. Das Lanthan-Kation La3+ ist ein positiver allosterischer Modulator an nativen und rekombinanten GABA-Rezeptoren, der die Zeit offener Kanäle erhöht und die Desensibilisierung in Abhängigkeit von der Konfiguration der Untereinheit verringert.[58]
Lanthan ist ein essentieller Cofaktor für die Methanoldehydrogenase des methanotrophen Bakteriums Methylacidiphilum fumariolicum SolV, obwohl die große chemische Ähnlichkeit der Lanthaniden bedeutet, dass es ohne negative Auswirkungen durch Cer, Praseodym oder Neodym ersetzt werden kann und das kleinere Samarium, Europium oder Gadolinium keine anderen Nebenwirkungen als ein langsameres Wachstum hervorruft.[59]
Vorsichtsmaßnahmen[edit]
Lanthan hat eine geringe bis mäßige Toxizität und sollte mit Vorsicht behandelt werden. Die Injektion von Lanthanlösungen führt zu Hyperglykämie, niedrigem Blutdruck, Degeneration der Milz und Leberveränderungen.[citation needed] Die Anwendung in Kohlenstoffbogenlicht führte dazu, dass Menschen Oxiden und Fluoriden von Seltenerdelementen ausgesetzt wurden, was manchmal zu Pneumokoniose führte.[61][62] Wie der La3+ Das Ion ist ähnlich groß wie das Ca.2+ In medizinischen Studien wird es manchmal als leicht nachvollziehbarer Ersatz für Letzteres verwendet.[63] Es ist bekannt, dass Lanthan wie die anderen Lanthaniden den menschlichen Stoffwechsel beeinflusst, den Cholesterinspiegel, den Blutdruck, den Appetit und das Risiko einer Blutgerinnung senkt. Wenn es in das Gehirn injiziert wird, wirkt es ähnlich wie Morphium und andere Opiate als Schmerzmittel, obwohl der Mechanismus dahinter noch unbekannt ist.[63]
Siehe auch[edit]
- ^ Es ist umstritten, ob Yttrium (Y) wirklich der leichtere Kongener von Lanthan (La) ist. Ein IUPAC-Projekt wurde am gestartet 18. Dezember 2015 zu empfehlen, ob es ist oder nicht.
Verweise[edit]
- ^ Meija, Juris; et al. (2016). “Atomgewichte der Elemente 2013 (IUPAC Technical Report)”. Reine und Angewandte Chemie. 88 (3): 265–91. doi:10.1515 / pac-2015-0305.
- ^ Yttrium und alle Lanthanoide mit Ausnahme von Ce und Pm wurden in der Oxidationsstufe 0 in Bis (1,3,5-tri-t-butylbenzol) -Komplexen beobachtet, siehe Cloke, F. Geoffrey N. (1993). “Zero Oxidation State Compounds von Scandium, Yttrium und den Lanthaniden”. Chem. Soc. Rev.. 22: 17–24. doi:10.1039 / CS9932200017. und Arnold, Polly L.; Petrukhina, Marina A.; Bochenkov, Vladimir E.; Shabatina, Tatyana I.; Zagorskii, Vyacheslav V.; Cloke (15.12.2003). “Arenkomplexierung von Sm-, Eu-, Tm- und Yb-Atomen: eine spektroskopische Untersuchung mit variabler Temperatur”. Zeitschrift für metallorganische Chemie. 688 (1–2): 49–55. doi:10.1016 / j.jorganchem.2003.08.028.
- ^ Lide, DR, hrsg. (2005). “Magnetische Suszeptibilität der Elemente und anorganischen Verbindungen”. CRC Handbuch für Chemie und Physik (PDF) (86. Ausgabe). Boca Raton (FL): CRC-Presse. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbuch für Chemie und Physik. Boca Raton, Florida: Verlag der Chemical Rubber Company. S. E110. ISBN 0-8493-0464-4.
- ^ https://www.britannica.com/science/lanthanum
- ^ https://www.angelo.edu/faculty/kboudrea/periodic/trans_transition.htm#:~:text=Group%203B%20(3)&text=In%20most%20periodic%20tables%2C%20lanthanum,lawrencium%20in % 20Gruppe% 203B% 20 statt
- ^
“Monazit- (Ce) Mineraldaten”. Webmineral. Abgerufen 10. Juli 2016. - ^ Greenwood und Earnshaw, p. 1102
- ^ ein b Greenwood und Earnshaw, p. 1106
- ^ ein b c d e f G h ich Patnaik, Pradyot (2003). Handbuch anorganischer chemischer Verbindungen. McGraw-Hill. S. 444–446. ISBN 978-0-07-049439-8. Abgerufen 2009-06-06.
- ^ Cullity, BD und Graham, CD (2011) Einführung in magnetische Materialien, John Wiley & Sons, ISBN 9781118211496
- ^ Wittig, Jörg (1973). “Die Druckvariable in der Festkörperphysik: Was ist mit 4f-Band-Supraleitern?” In HJ Queisser (Hrsg.). Festkörper Probleme: Plenarvorträge der Abteilungen Halbleiterphysik, Oberflächenphysik, Niedertemperaturphysik, Hochpolymere, Thermodynamik und statistische Mechanik der Deutschen Physikalischen Gesellschaft, Münster, 19.-24. März 1973. Fortschritte in der Festkörperphysik. 13. Berlin, Heidelberg: Springer. S. 375–396. doi:10.1007 / BFb0108579. ISBN 978-3-528-08019-8.
- ^ Gschneidner Jr., Karl A. (2016). “282. Systematik”. In Jean-Claude G. Bünzli; Vitalij K. Pecharsky (Hrsg.). Handbuch zur Physik und Chemie der Seltenen Erden. 50. S. 12–16. ISBN 978-0-444-63851-9.
- ^ Krishnamurthy, Nagaiyar und Gupta, Chiranjib Kumar (2004) Extraktive Metallurgie der Seltenen Erden, CRC Press, ISBN 0-415-33340-7
- ^ Greenwood und Earnshaw, p. 1429
- ^ ein b c d e f Lide, DR, hrsg. (2005). CRC Handbuch für Chemie und Physik (86. Ausgabe). Boca Raton (FL): CRC-Presse. ISBN 0-8493-0486-5.
- ^ Die Radiochemie der Seltenen Erden, Scandium, Yttrium und Actinium
- ^ Greenwood und Earnshaw, p. 1105–7
- ^ “Seltenerdmetall-Langzeit-Luftbelastungstest”. Abgerufen 08.08.2009.
- ^ ein b “Chemische Reaktionen von Lanthan”. Webelements. Abgerufen 2009-06-06.
- ^ Greenwood und Earnshaw, p. 1434
- ^ ein b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), “DannUBASE Bewertung der Kern- und Zerfallseigenschaften “, Kernphysik A., 729: 3–128, Bibcode:2003NuPhA.729 …. 3A, doi:10.1016 / j.nuclphysa.2003.11.001
- ^ Woosley, SE; Hartmann, DH; Hoffman, RD; Haxton, WC (1990). “Der ν-Prozess”. Das astrophysikalische Journal. 356: 272–301. doi:10.1086 / 168839.
- ^ ein b c d Greenwood und Earnshaw, p. 1107–8
- ^ Fukai, Y. (2005). Das Metall-Wasserstoff-System, Basic Bulk Properties, 2. Auflage. Springer. ISBN 978-3-540-00494-3.
- ^ ein b Greenwood and Earnshaw, S. 1108–9
- ^ Greenwood und Earnshaw, p. 1110
- ^ “Die Entdeckung und Benennung der Seltenen Erden”. Elements.vanderkrogt.net. Abgerufen 23. Juni 2016.
- ^ ein b Greenwood und Earnshaw, p. 1424
- ^ Weeks, Mary Elvira (1956). Die Entdeckung der Elemente (6. Aufl.). Easton, PA: Journal of Chemical Education.
- ^ Weeks, Mary Elvira (1932). “Die Entdeckung der Elemente: XI. Einige mit Hilfe von Kalium und Natrium isolierte Elemente: Zirkonium, Titan, Cer und Thorium”. Das Journal of Chemical Education. 9 (7): 1231–1243. Bibcode:1932JChEd … 9.1231W. doi:10.1021 / ed009p1231.
- ^ Sehen:
- (Berzelius) (1839) “Nouveau métal” (Neues Metall), Comptes rendus, 8 : 356-357. Ab p. 356: “L’oxide de cérium, extrait de la cérite par la procédé ordinaire, Kontient à peu près les deux cinquièmes de son poids de l’oxide du nouveau métal qui ne change que peu les propriétés du cérium et qui s’y tient pour ainsi dire caché. Cette raison a engagé M. Mosander à donner au nouveau métal le nom de Lantane. “ (Das nach dem üblichen Verfahren aus Cerit extrahierte Ceroxid enthält fast zwei Fünftel seines Gewichts im Oxid des neuen Metalls, das sich nur geringfügig von den Eigenschaften des Cer unterscheidet und sozusagen “verborgen” darin gehalten wird “. Dieser Grund motivierte Herrn Mosander, dem neuen Metall den Namen zu geben Lantane.)
- (Berzelius) (1839) “Latanium – ein neues Metall” Philosophisches Magazin, Neue Serien, 14 : 390-391.
- ^
“Es ist elementar – das Periodensystem der Elemente”. Jefferson Lab. Archiviert vom Original am 29. April 2007. Abgerufen 2007-04-14. - ^
Hudson Institute of Mineralogy (1993–2018). “Mindat.org”. www.mindat.org. Abgerufen 14. Januar 2018. - ^ Greenwood und Earnshaw, p. 1103
- ^ ein b c Greenwood und Earnshaw, p. 1426–9
- ^ Evans, CH, ed. (2012-12-06). Episoden aus der Geschichte der Seltenerdelemente. Kluwer Academic Publishers. p. 122. ISBN 9789400902879.
- ^ “In der Nickel-Metallhydrid-Batterie” (PDF). Archiviert von das Original (PDF) am 27.02.2009. Abgerufen 2009-06-06.
- ^ Tliha, M.; Mathlouthi, H.; Lamloumi, J.; Percheronguegan, A. (2007). “Wasserstoffspeicherlegierung vom Typ AB5, die als anodische Materialien in Ni-MH-Batterien verwendet wird”. Zeitschrift für Legierungen und Verbindungen. 436 (1–2): 221–225. doi:10.1016 / j.jallcom.2006.07.012.
- ^ “Wenn Hybridautos seltene Metalle verschlingen, droht ein Mangel”. Reuters 31.08.2009. 2009-08-31.
- ^ Bauerlein, P.; Antonius, C.; Loffler, J.; Kumpers, J. (2008). “Fortschritte bei Hochleistungs-Nickel-Metallhydrid-Batterien”. Journal of Power Sources. 176 (2): 547. Bibcode:2008JPS … 176..547B. doi:10.1016 / j.jpowsour.2007.08.052.
- ^ “Warum Toyota im nächsten Prius 2 Batterieoptionen anbietet”.
- ^ Uchida, H. (1999). “Wasserstofflöslichkeit in Wasserstoffspeicherlegierungen auf Seltenerdbasis”. Internationale Zeitschrift für Wasserstoffenergie. 24 (9): 871–877. doi:10.1016 / S0360-3199 (98) 00161-X.
- ^ CR Hammond (2000). Die Elemente im Handbuch für Chemie und Physik (81. Ausgabe). CRC drücken. ISBN 978-0-8493-0481-1.
- ^ Jason D. Sommerville und Lyon B. King. “Einfluss der Kathodenposition auf die Leistung des Hall-Effekt-Triebwerks und die Kathodenkopplungsspannung” (PDF). 43. Gemeinsame Antriebskonferenz und Ausstellung AIAA / ASME / SAE / ASEE, 8.-11. Juli 2007, Cincinnati, OH. Archiviert von das Original (PDF) am 20. Juli 2011. Abgerufen 2009-06-06.
- ^ Harrington, James A. “Infrarot-Glasfaser” (PDF). Rutgers Universität. Archiviert von das Original (PDF) am 02.08.2010.
- ^ “BrilLanCe-NxGen” (PDF). Archiviert von das Original (PDF) am 29.04.2011. Abgerufen 2009-06-06.
- ^ Hendrick, James B. (1985). “Seltenerdelemente und Yttrium”. Mineralische Fakten und Probleme (Bericht). Bureau of Mines. p. 655. Bulletin 675.
- ^ Kim, K; Shim, Kwang Bo (2003). “Die Wirkung von Lanthan auf die Herstellung von ZrB2-ZrC-Verbundwerkstoffen durch Funkenplasmasintern”. Materialcharakterisierung. 50: 31–37. doi:10.1016 / S1044-5803 (03) 00055-X.
- ^ Grundlagen der Poolpflege. S. 25–26.
- ^ Howard B. Cary (1995). Automatisierung des Lichtbogenschweißens. CRC Drücken Sie. p. 139. ISBN 978-0-8247-9645-7.
- ^ Larry Jeffus. (2003). “Arten von Wolfram”. Schweißen: Prinzipien und Anwendungen. Clifton Park, NY: Thomson / Delmar-Lernen. p. 350. ISBN 978-1-4018-1046-7. Archiviert von das Original am 23.09.2010.
- ^ CK Gupta; Nagaiyar Krishnamurthy (2004). Extraktive Metallurgie von Seltenen Erden. CRC Drücken Sie. p. 441. ISBN 978-0-415-33340-5.
- ^ S. Nakai; A. Masuda; B. Lehmann (1988). “La-Ba-Datierung von Bastnaesit” (PDF). Amerikanischer Mineralogist. 7 (1–2): 1111. Bibcode:1988ChGeo..70 … 12N. doi:10.1016 / 0009-2541 (88) 90211-2.
- ^ ein b “Die FDA genehmigt Fosrenol (R) bei Patienten mit Nierenerkrankungen im Endstadium (ESRD).”. 28. Oktober 2004. Abgerufen 2009-06-06.
- ^ Chau YP; Lu KS (1995). “Untersuchung der Blutganglienbarriereeigenschaften in sympathischen Ganglien von Ratten unter Verwendung von Lanthanionen und Meerrettichperoxidase als Tracer”. Acta Anatomica. 153 (2): 135–144. doi:10.1159 / 000313647. ISSN 0001-5180. PMID 8560966.
- ^ Hagheseresht; Wang, Shaobin; Do, DD (2009). “Ein neuartiger Lanthan-modifizierter Bentonit, Phoslock, zur Phosphatentfernung aus Abwässern”. Angewandte Tonwissenschaft. 46 (4): 369–375. doi:10.1016 / j.clay.2009.09.009.
- ^ Boldyreva, AA (2005). “Lanthan potenziert GABA-aktivierte Ströme in Rattenpyramiden-Neuronen des CA1-Hippocampusfeldes”. Bulletin für Experimentelle Biologie und Medizin. 140 (4): 403–5. doi:10.1007 / s10517-005-0503-z. PMID 16671565. S2CID 13179025.
- ^ Pol, Arjan; Barends, Thomas RM; Dietl, Andreas; Khadem, Ahmad F.; Eygensteyn, Jelle; Jetten, Mike SM; Op Den Camp, Huub JM (2013). “Seltenerdmetalle sind für das methanotrophe Leben in vulkanischen Schlammtöpfen unerlässlich”. Umweltmikrobiologie. 16 (1): 255–64. doi:10.1111 / 1462-2920.12249. PMID 24034209.
- ^ “Lanthan 261130”. Sigma-Aldrich.
- ^ Dufresne, A.; Krier, G.; Muller, J.; Case, B.; Perrault, G. (1994). “Lanthanoidpartikel in der Lunge eines Druckers”. Wissenschaft der gesamten Umwelt. 151 (3): 249–252. Bibcode:1994ScTEn.151..249D. doi:10.1016 / 0048-9697 (94) 90474-X. PMID 8085148.
- ^ Waring, PM; Watling, RJ (1990). “Seltenerdablagerungen in einem verstorbenen Filmvorführer. Ein neuer Fall von Seltenerdpneumokoniose”. Das Medical Journal of Australia. 153 (11–12): 726–30. doi:10.5694 / j.1326-5377.1990.tb126334.x. PMID 2247001. S2CID 24985591.
- ^ ein b Emsley, John (2011). Bausteine der Natur: Ein AZ-Leitfaden zu den Elementen. Oxford University Press. S. 266–77. ISBN 9780199605637.
Literaturverzeichnis[edit]
Weiterführende Literatur[edit]
- Die industrielle Chemie der Lanthanonen, Yttrium, Thorium und Uranvon RJ Callow, Pergamon Press, 1967
- Extraktive Metallurgie der Seltenen Erden, von CK Gupta und N. Krishnamurthy, CRC Press, 2005
- Nouveau Traite de Chimie Minerale. VII. Scandium, Yttrium, Elements des Terres Rares, ActiniumP. Pascal, Herausgeber, Masson & Cie, 1959
- Chemie der Lanthanonsvon RC Vickery, Butterworths 1953
Recent Comments