ガリウムヒドロキシド – ウィキペディア
before-content-x4
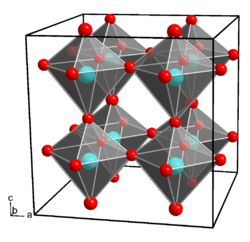
| 結晶構造 | |
|---|---|
 |
|
| _ ために 3+ _ おお – | |
| 全般的 | |
| 名前 | ガリウムヒドロキシド |
| 他の名前 |
|
| 比率式 | GA(ああ) 3 |
| 簡単な説明 |
無色のアモルファス塊 [初め] または結晶物質 [2] |
| 外部識別子/データベース | |
| 特性 | |
| モル質量 | 120.74 g・mol -1 |
| 総状態 |
祭り |
| 密度 |
3,84 g・cm -3 [3] |
| 溶解度 |
希釈鉱酸に可溶 [4] |
| 安全についての案内 | |
| 可能な限り一般的に、SIユニットが使用されます。特に明記しない限り、提供されたデータは標準条件に適用されます。 | |
ガリウムヒドロキシド ハイドロキシドのグループからのガリウムの化学的接続です。
ガリウム水酸化は自然に鉱物の息子として発生します。 [6]
ガリウムはガリウム(III)塩溶液の中和で発生します。 [初め] ガリウム水酸化物は、アルミニウム抽出のドーム生成物として落ちます。 [7]
- [初め] または無色の矯正矯正矯正および擬似クバンの結晶物質として。 [2] 水酸化ガリウムに加えて、ガリウム(III)酸化酸化一水酸塩(GAO(OH)またはGA 2 o 3 •h 2 o)ガリウムの他の水酸化物(酸化ガリウム水酸化物)を参照する [初め] 、水酸化ガリウムで加熱すると約170°Cです [4] 、熱水条件下で50 kbarで900°Cに加熱するか、ゆっくりと老化によって引き起こされます。 500°Cを超える加熱により、ガリウム(III)酸化物の形成の下で分解します。 [7]
ガリウム水酸化物は、矯正結晶系、ルームグループで結晶化します PMN 2 初め (部屋グループ番号31) 、グリッドパラメーターを使用します a = 7,487に b = 7,438からund c = 7,496 to。 [8] 各ガリウム原子は、6つのヒドロキシジョンによって調整され、各ヒドロキシディオンは2つのガリウムイオンに結合します。
硫化水素との反応により、ガリウム(III)硫化物を得ることができます。 [9]
- ↑ a b c d 化学技術のKirk-Othmer百科事典: ガリウムおよびガリウム化合物 ( 記念 2012年4月27日から インターネットアーカイブ ))
- ↑ a b HandbookofMineralogy: 息子 (PDF; 70 kb)
- ↑ ジャン・ダン、エレン・ラックス。化学者と物理学者向けのペーパーバック:第3巻、p。464; ISBN 978-3540600350
- ↑ a b Georg Brauer(編)、Marianne Baudlerのコラボレーションと。: 検体無機化学のハンドブック。 3番目、改訂版。第2巻、フェルディナンド・エンケ、シュトゥットガルト1978、ISBN 3-432-87813-3、p。855。
- ↑ この物質の調和の分類はまだありません。伝統的な魅力による自己分類のラベル付けが再現されます ガリウムトリヒドロキシド の中に 分類およびラベル付けインベントリ 2020年5月26日にアクセスされた欧州化学機関(ECHA)。
- ↑ ミネラルアトラス:Söhngeit
- ↑ a b A. F.ホレマン、E。ウィバーグ、N。ウィバーグ: 無機化学の教科書。 102.エディション。 Walter de Gruyter、Berlin 2007、ISBN 978-3-11-017770-1、p。1196。
- ↑ J.D.スコット: 新しいミネラルの結晶構造、ソンゲート。 の: アメリカの鉱物学者 、56、1871、S。355。
- ↑ Georg Brauer、Marianne BaudlerとAのコラボレーションと。 (編): 検体無機化学のハンドブック 。 3番目、改訂版。 バンド 初め 。 Ferdinand Entemp、1975年のシュトゥッガート、ISBN 3-4 3-432-02328-6、 S. 857 。
after-content-x4
 [初め] または無色の矯正矯正矯正および擬似クバンの結晶物質として。 [2] 水酸化ガリウムに加えて、ガリウム(III)酸化酸化一水酸塩(GAO(OH)またはGA 2 o 3 •h 2 o)ガリウムの他の水酸化物(酸化ガリウム水酸化物)を参照する [初め] 、水酸化ガリウムで加熱すると約170°Cです [4] 、熱水条件下で50 kbarで900°Cに加熱するか、ゆっくりと老化によって引き起こされます。 500°Cを超える加熱により、ガリウム(III)酸化物の形成の下で分解します。 [7]
[初め] または無色の矯正矯正矯正および擬似クバンの結晶物質として。 [2] 水酸化ガリウムに加えて、ガリウム(III)酸化酸化一水酸塩(GAO(OH)またはGA 2 o 3 •h 2 o)ガリウムの他の水酸化物(酸化ガリウム水酸化物)を参照する [初め] 、水酸化ガリウムで加熱すると約170°Cです [4] 、熱水条件下で50 kbarで900°Cに加熱するか、ゆっくりと老化によって引き起こされます。 500°Cを超える加熱により、ガリウム(III)酸化物の形成の下で分解します。 [7]


Recent Comments