正式な貨物 – 無料百科事典
化学では、a 正式な負荷 ( Q f )それは分子内の原子の部分的な負荷であり、化学結合内の電子が反対電気陰性度を考慮せずに、原子間で等しく共有されていると仮定することによって割り当てられています [ 初め ] または、別の定義では、すべてのリガンドがホモリティックに除去されたときに原子にある負荷。 [ 2 ]
分子内の任意の原子の正式な負荷は、次の方程式で計算できます。
どこ:
- 自由原子の価電子の数です。
- それは、孤独なペアとして付着した原子に存在する電子の数です。
- 原子に付着した電子の数です。
正しいルイス構造(または共鳴構造)が分子に対して決定される場合、それは各原子の正式な負荷(符号なし)が最小化される最終構造の選択における非常に重要な基準です。

例
- メタン中の炭素(Cho 4 ):Q f = 4-0-(8÷2)= 0
- ニトログループの窒素(いいえ 2 – ):Q f = 5-0-(8÷2)= 0
- NOの単純なリンクによって取り付けられた酸素 2 – :Q f = 6-5-(2÷2)= 0
- No 2 – :Q f = 6-4-(4÷2)= 0
電気陰性度を考慮して原子に負荷を割り当てる代替方法は、その酸化数によるものです。他の関連する概念はバレンシアです。バレンシアは、原子がリンクで使用する電子の数と、対象原子に統合された原子の数を調整数を持つバレンシアです。
アンモニウム(NH 4 + )それは陽イオン種です。周期表で原子の垂直グループを使用する場合、各水素が1電子に寄与することを判断することができ、窒素は5つの電子に寄与し、+1荷重は1電子が存在しないことを意味します。最終合計は8電子です
。
ルイス構造を描くことで、SPでハイブリダイズした窒素原子が得られます 3 (4つの結合)水素原子に囲まれた。電子フリーペアはありません。その結果、正式な負荷の定義を適用すると、水素には正式なゼロ負荷があります。
、および窒素には+1の正式な負荷があります:
。分子全体にすべての正式な負荷を追加した後、結果は最初に与えられた分子の負荷で構成される+1の正式な負荷になります。
注:分子の総正式な負荷は、可能な限り最小の負荷でゼロにできるだけ近い必要があります
- 例:co 2 これは、16の総価電子電子を持つ中性分子です。ルイス構造を描くには3つの異なる方法があります
- 各酸素原子への単純な結合によって取り付けられた炭素原子(炭素= +2、酸素= -1、合計形式荷重= 0)
- 酸素原子への単純な結合によって取り付けられ、もう一方は二重結合によって取り付けられています(炭素= +1、酸素 ダブル = 0、酸素 単純 = -1、合計正式な負荷= 0)
- 両方の酸素原子に二重結合によって取り付けられた炭素原子(炭素= 0、酸素= 0、合計形式荷重= 0)
3つの構造は総負荷を与えますが、分子に負荷がないため、正しい構造は3番目です。
代替方法 [ 編集します ]
上記の式は正しいものですが、通常は処理するのが難しく、使用は非効率的です。代替方法は次のとおりです。
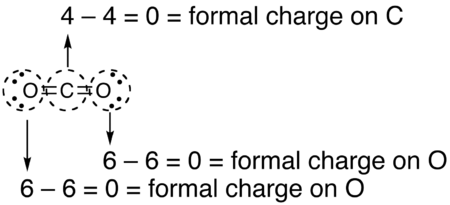
- 正式な負荷が必要な原子の周りに円を描きます(二酸化炭素のように、下の)
- 原子の円の中の電子の数を数えます。円は共有結合を「半分に」切断するため、各共有結合は2つではなく単一の電子としてカウントされます。
- グループのグループ数(IUPACの1-18システムではなく、以前のグループ番号システムのローマ数字)の円の電子の数を減算して、正式な負荷を決定します。 (つまり、グループの古い数は円の電子から電子を引いたものです)
- 二酸化炭素のこのルイス構造の残りの原子について計算された正式な負荷を以下に示します
繰り返しますが、この方法は前の方法と同じくらい正確ですが、より簡単に使用します。正式な請求はだけであることに留意することが重要です 丁寧 、このシステムは単なる形式主義であるという意味で。
分子の原子には、負荷を示す「首の周りの兆候」がありません。正式な荷重システムは、分子が形成されたときに各原子がそれにもたらすすべての原子価電子のアカウントを保持する方法にすぎません。
正式な負荷対酸化状態 [ 編集します ]
酸化状態の概念は、分子内の電子の分布を決定する有能な方法を構成します。原子の正式な負荷と酸化状態が二酸化炭素で比較される場合、次の値に達します。
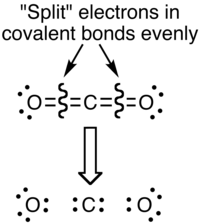
これらの値の違いの理由は、正式な負荷と酸化状態が主に分子の原子内の電子の分布を評価するさまざまな方法を表しているためです。正式な負荷では、各共有結合の電子がリンク内の2つの原子の間に等しい部分で分離されていると想定されています(したがって、上記の2つの方法の間の分割が発生します)。 COの正式な負荷の視点 2 基本的に以下に示されています:
炭素原子と比較して、電気陰性度が高いため、実際には酸素原子の周りにより大きな電子密度があるため、結合の共有結合の側面(共有)は正式な負荷の使用において過剰に署名されています。これは、電位マップでより効果的に視覚化できます。
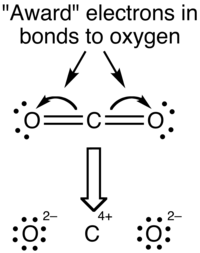
酸化状態の形式主義により、結合内の電子は、より大きな電気陰性度の原子に「付与」されます。 CO分子の酸化状態の視点 2 下に示された:
酸化状態は、リンクのイオン性を克服します。化学物質の大部分は、炭素と酸素の間の電気陰性度の違いは、結合がイオン性であるかのように考慮するには不十分であることに同意しています。
実際、分子内の電子の分布は、これら2つの端の間のある時点にあります。分子のルイス構造の単純なビジョンの不十分さは、より一般的な用途モデルとより大きな精度の発達につながりました。バレンシア・デ・スレーター、ポーリングなどの理論、そしてロバート・S・マリエンとハウンドによって開発された分子軌道の理論まで。
参照 [ 編集します ]
外部リンク [ 編集します ]
- 正式な料金 @ジョージアサザン大学 リンク
- ミシガン州立大学 @ミシガン州立大学 リンク アーカイブ 2010年2月12日、Wayback Machineで。
- さらに正式な充電演習 @サザンメイン大学 リンク




 。
。  、および窒素には+1の正式な負荷があります:
、および窒素には+1の正式な負荷があります:  。分子全体にすべての正式な負荷を追加した後、結果は最初に与えられた分子の負荷で構成される+1の正式な負荷になります。
。分子全体にすべての正式な負荷を追加した後、結果は最初に与えられた分子の負荷で構成される+1の正式な負荷になります。 

Recent Comments