 |
|
 |
|
| Tên | |
|---|---|
| Tên IUPAC ưa thích
Natri tetrahydridobISE (1 -) |
|
| Tên IUPAC có hệ thống | |
| Mã định danh | |
| ChEBI | |
| ChemSpider | |
| Thẻ thông tin ECHA | 100.037.262 |
| Số EC | 241-004-4 |
| 23167 | |
| MeSH | Natri + borohydride |
| Số RTECS | ED3325000 |
| Số UN | 1426 |
|
|
| Thuộc tính | |
| NaBH 4 | |
| Khối lượng mol | 37,83 g / mol |
| Xuất hiện | tinh thể trắng hút ẩm |
| Mật độ | 1.0740 g / cm 3 |
| Điểm nóng chảy | 400 ° C (752 ° F; 673 K) [1] |
| Điểm sôi | 500 ° C (932 ° F; 773 K) (bị phân hủy) [1] |
| hòa tan, phản ứng với nước | |
| Độ hòa tan | hòa tan trong amoniac lỏng, amin, pyridin |
| Nguy cơ | |
| H260 H602 H311 H314 | |
| P223 P231 P232 P280 P495 + 310 378 P422 | |
| NFPA 704 |
] |
| Điểm chớp cháy | 70 ° C (158 ° F; 343 K) |
| ca. 220 ° C (428 ° F; 493 K) | |
| Giới hạn nổ | 3% |
| Liều hoặc nồng độ gây chết người ( LD LC ): | |
| 160 mg / kg (uống – chuột) 230 mg / kg (Dermal – Rabbit) |
|
| Các hợp chất liên quan | |
| Natri cyanoborohydride Natri hydrua Natri borat Borax |
|
| Lithium borohydride | |
|
Các hợp chất liên quan |
Hydride nhôm nhôm Natri triacetoxyborohydride |
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu ở trạng thái tiêu chuẩn của chúng (ở 25 ° C [77 °F]100 kPa).
|
|
| Tham chiếu hộp thông tin | |
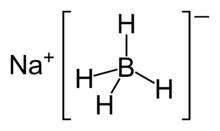
Natri borohydride còn được gọi là natri tetrahydridoborate và natri tetrahydroborate [2] là một hợp chất vô cơ có công thức NaBH Chất rắn màu trắng này, thường gặp dưới dạng bột, là chất khử tìm thấy ứng dụng trong hóa học, cả trong phòng thí nghiệm và trên quy mô kỹ thuật. Nó đã được thử nghiệm như tiền xử lý để nghiền gỗ, nhưng quá tốn kém để được thương mại hóa. [3][4] Hợp chất này hòa tan trong rượu, một số ete nhất định và thậm chí cả nước, mặc dù nó bị thủy phân chậm [5]
Hợp chất được phát hiện vào những năm 1940 bởi HI Schlesinger, người lãnh đạo một nhóm tìm kiếm các hợp chất urani dễ bay hơi. [6] Kết quả của nghiên cứu thời chiến này đã được giải mật và công bố vào năm 1953.
Thuộc tính [ chỉnh sửa ]
| Dung môi | Độ hòa tan (g / 100 mL) [5] |
|---|---|
| MeOH | 13 |
| EtOH | 3.16 |
| Diglyme | 5.15 |
| Et 2 O | không hòa tan |
Natri borohydride là một loại bột vi tinh thể màu trắng đến xám trắng thường tạo thành cục. Nó có thể được tinh chế bằng cách kết tinh lại từ diglyme ấm (50 ° C). [7] Natri borohydride hòa tan trong dung môi protic như nước và rượu thấp hơn. Nó cũng phản ứng với các dung môi protic này để tạo ra H 2 tuy nhiên, những phản ứng này khá chậm. Quá trình phân hủy hoàn toàn dung dịch metanol cần gần 90 phút ở 20 ° C. [8] Nó sẽ bị phân hủy trong dung dịch nước trung tính hoặc axit, nhưng ổn định ở pH 14. [5]
Cấu trúc [ chỉnh sửa ]
NaBH 4 là một loại muối, bao gồm tứ diện BH 4 – anion. Chất rắn được biết là tồn tại dưới dạng ba đa hình: α β và . Pha ổn định ở nhiệt độ và áp suất phòng là α -NaBH 4 là khối và áp dụng cấu trúc kiểu NaCl, trong nhóm không gian Fm3m . Ở áp suất 6,3 GPa, cấu trúc thay đổi thành tứ giác β -NaBH 4 (nhóm không gian P42 1 c ) 8,9 GPa, trực giao γ -NaBH 4 (nhóm không gian Pnma ) trở nên ổn định nhất. [9][10][11]
| Để sản xuất NaBH4 thương mại và quy trình của Bayer là những phương pháp phổ biến nhất. Trong quy trình Brown-Schlesinger, Natri borohydride được điều chế công nghiệp theo phương pháp Schlesinger ban đầu: natri hydrua (được tạo ra bằng phản ứng Na và H2) được xử lý bằng trimethyl borat ở 250 nhiệt270 ° C:
Hàng triệu kilôgam được sản xuất hàng năm vượt xa mức sản xuất của bất kỳ chất khử hydrua nào khác. [3] Natri borohydride cũng có thể được sản xuất do tác dụng của NaH trên thủy tinh borosilicate dạng bột. [12] Khác với quy trình này, quy trình của Bayer dựa trên phản ứng giữa borax (Na 2 B 4 O 7 ), Na, H 2 và oxit silic (SiO 2 ) tại 700 ° C để tổng hợp NaBH 4 :
Hiện tại có một nỗ lực để sửa đổi Quy trình của Bayer bằng cách sử dụng magiê kim loại (Mg) ít tốn kém hơn trong nơi chứa natri. Các phản ứng như:
và
đang hứa hẹn sửa đổi cho Quy trình của Bayer, nhưng chưa được phát triển đủ để thể hiện cả năng suất cao và tốc độ phản ứng nhanh. [13][14] Độ phản ứng [ chỉnh sửa ]NaBH 4 sẽ làm giảm nhiều carbonyl hữu cơ, tùy thuộc vào các điều kiện chính xác. Thông thường nhất, nó được sử dụng trong phòng thí nghiệm để chuyển đổi ketone và aldehyd thành rượu. Nó sẽ làm giảm hiệu quả acyl clorua, anhydrid, α-hydroxylactones, thioesters và bắt chước ở nhiệt độ phòng hoặc thấp hơn. Nó sẽ làm giảm este từ từ và không hiệu quả với thuốc thử dư thừa và / hoặc nhiệt độ tăng cao, trong khi axit cacboxylic và amit không bị giảm chút nào. [15] NaBH 4 phản ứng với nước và rượu, với sự phát triển của khí hydro và rượu. hình thành muối borat, phản ứng đặc biệt nhanh ở pH thấp. Tuy nhiên, một loại rượu, thường là metanol hoặc ethanol, thường là dung môi được lựa chọn để khử natri borohydride của ketone và aldehyd. Cơ chế khử ketone và aldehyd đã được nghiên cứu kỹ lưỡng bởi các nghiên cứu động học, và trái với các mô tả phổ biến trong sách giáo khoa, cơ chế này không liên quan đến trạng thái chuyển tiếp 4 thành viên như hydrat hóa kiềm, [16] hoặc trạng thái chuyển tiếp sáu thành viên liên quan đến một phân tử của dung môi rượu. [17] Cần phải kích hoạt liên kết hydro, vì không xảy ra sự khử trong dung môi không proton như diglyme. Tuy nhiên, thứ tự tỷ lệ trong rượu là 1,5, trong khi hợp chất carbonyl và borohydride đều là thứ tự đầu tiên, cho thấy một cơ chế phức tạp hơn một cơ chế liên quan đến trạng thái chuyển tiếp sáu thành viên chỉ bao gồm một phân tử rượu duy nhất. Có ý kiến cho rằng sự kích hoạt đồng thời của hợp chất carbonyl và borohydride xảy ra, thông qua tương tác với ion rượu và kiềm, tương ứng, và phản ứng tiến hành thông qua trạng thái chuyển tiếp mở. [18] [19] α, β-ketone không bão hòa có xu hướng giảm bởi NaBH 4 theo nghĩa 1,4, mặc dù hỗn hợp thường được hình thành. Bổ sung xeri clorua như một chất phụ gia giúp cải thiện đáng kể tính chọn lọc đối với việc giảm 1,2 xeton không bão hòa (giảm Luche). Các este α, β-chưa bão hòa cũng trải qua quá trình khử 1,4 khi có mặt NaBH 4 . [5] Nhiều thuốc thử hydrua khác đang giảm mạnh hơn. Chúng thường liên quan đến việc thay thế hydride bằng các nhóm alkyl, chẳng hạn như lithium triethylborohydride và L-Selectride (lithium tri- giây -butylborohydride) hoặc thay thế B bằng Al. Các biến thể trong phản ứng cũng ảnh hưởng đến khả năng phản ứng của borohydride. [20] Khả năng phản ứng của NaBH 4 có thể được tăng cường hoặc tăng cường bởi nhiều loại hợp chất. với iốt trong tetrahydrofuran tạo ra phức hợp tetrahydrofuran borane, có thể làm giảm axit cacboxylic. [23] Tương tự như vậy, hệ thống NaBH 4 -MeOH, được hình thành bằng cách thêm metanol vào natri borohydride. với các rượu tương ứng. [24] Trộn nước hoặc rượu với borohydride chuyển một phần của nó thành este hydride không ổn định, hiệu quả hơn trong việc khử, nhưng chất khử cuối cùng sẽ tự phân hủy để tạo ra khí hydro và borat. Phản ứng tương tự cũng có thể xảy ra nội phân tử: một α-ketoester chuyển thành diol, do rượu được tạo ra sẽ tấn công borohydride để tạo ra este của borohydride, sau đó làm giảm este lân cận. [25] Sự kết hợp của NaBH 4 với axit cacboxylic dẫn đến sự hình thành các loài acyloxyborohydride, chẳng hạn như STAB. Những chất này có thể thực hiện nhiều loại khử khác nhau thường không liên quan đến hóa học borohydride, chẳng hạn như rượu thành hydrocacbon và nitriles thành các amin chính. [26] Hóa học phối hợp [ chỉnh sửa ]BH – là một phối tử cho các ion kim loại. Các phức borohydride như vậy thường được điều chế bằng tác dụng của NaBH 4 (hoặc LiBH 4 ) trên halogen kim loại tương ứng. Một ví dụ là dẫn xuất titanocen: [27]
Nguồn hydro [ chỉnh sửa ]với sự có mặt của chất xúc tác kim loại , natri borohydride giải phóng hydro. Khai thác khả năng phản ứng này, natri borohydride được sử dụng trong các nguyên mẫu của pin nhiên liệu borohydride trực tiếp. Hydro được tạo ra cho pin nhiên liệu bằng cách phân hủy xúc tác của dung dịch borohydride nước:
|
