Viêm cầu thận phân đoạn khu trú ( FSGS ) là một nguyên nhân gây ra hội chứng thận hư ở trẻ em và thanh thiếu niên, cũng là nguyên nhân hàng đầu gây suy thận ở người lớn. [1] Nó còn được gọi là " xơ cứng cầu thận khu trú "hoặc" xơ hóa cầu thận khu trú. "[2] Nó chiếm khoảng một phần sáu các trường hợp hội chứng thận hư. [3] (Bệnh thay đổi tối thiểu (MCD) là nguyên nhân phổ biến nhất của hội chứng thận hư ở trẻ em: MCD và FSGS chính có thể có nguyên nhân tương tự. [1])
Phân loại [ chỉnh sửa ]
Tùy thuộc vào nguyên nhân, nó được phân loại rộng rãi là:
- Chính, khi không tìm thấy nguyên nhân cơ bản; thường biểu hiện như hội chứng thận hư
- Thứ phát, khi xác định được nguyên nhân cơ bản; thường biểu hiện với suy thận và protein niệu. Đây thực sự là một nhóm không đồng nhất bao gồm nhiều nguyên nhân như
Ngoài ra còn có nhiều chương trình phân loại khác.
Các biến thể bệnh lý [ chỉnh sửa ]
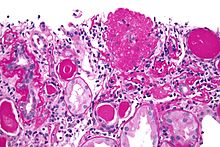
Năm biến thể loại trừ lẫn nhau của bệnh cầu thận phân đoạn khu trú có thể được phân biệt bằng các phát hiện bệnh lý được thấy trên sinh thiết thận: [4]
- biến thể tổn thương
- Biến thể tế bào
- Biến thể Perihilar
- Biến thể không được chỉ định khác (NOS).
Việc nhận biết các biến thể này có thể có giá trị tiên lượng ở những cá nhân mắc bệnh viêm cầu thận phân đoạn nguyên phát . Biến thể sụp đổ có liên quan đến tốc độ tiến triển cao hơn đối với bệnh thận ở giai đoạn cuối, trong khi biến thể tổn thương đầu cầu thận có tỷ lệ tiến triển thấp sang bệnh thận giai đoạn cuối ở hầu hết bệnh nhân. Biến thể tế bào cho thấy biểu hiện lâm sàng tương tự với biến thể sụp đổ và đầu cầu thận nhưng có kết quả trung gian giữa hai biến thể này. Tuy nhiên, do sự sụp đổ và biến thể đầu cầu thận cho thấy các đặc điểm bệnh lý chồng chéo với biến thể tế bào, sự khác biệt trung gian về kết quả lâm sàng này có thể phản ánh sai lệch lấy mẫu trong các trường hợp của bệnh viêm cầu thận phân đoạn khu trú tế bào (biến thể sụp đổ không biến dạng hoặc biến thể đầu cầu thận). Ý nghĩa tiên lượng của các biến thể perihilar và NOS vẫn chưa được xác định. Biến thể NOS là kiểu con phổ biến nhất. Biến thể sập là loại bệnh cầu thận phổ biến nhất do nhiễm HIV.
Một số nguyên nhân thứ phát chung được liệt kê dưới đây:
- Phì đại / phì đại cầu thận
- Cận thận đơn phương
- Bệnh béo phì
- Sẹo do chấn thương trước đó .
Viêm cầu thận phân đoạn khu trú có thể phát triển sau khi mất nephron do bệnh thận do trào ngược. Protein niệu là không chọn lọc trong hầu hết các trường hợp và có thể nằm trong phạm vi cận lâm sàng (phạm vi thận <3.0gm / 24 giờ) hoặc phạm vi thận. [6]
Nguyên nhân di truyền [ chỉnh sửa nguyên nhân di truyền của các hình thức di truyền của FSGS.
Gene
OMIM
Mô tả
FSGS1: ACTN4
603278
Gen đầu tiên liên quan đến rối loạn này là ACTN4, mã hóa alpha-actinin 4. Loại liên kết ngang protein này của các sợi Actin và có trong podocyte. Đột biến trong protein này liên quan đến FSGS dẫn đến tăng ái lực với liên kết Actin, hình thành các tập hợp nội bào và giảm thời gian bán hủy protein. Mặc dù không rõ làm thế nào những hiệu ứng này có thể dẫn đến FSGS, có một số lý thuyết. Thứ nhất, tập hợp protein có thể có tác dụng độc hại đối với podocyte. Thứ hai, giảm nửa đời protein hoặc tăng ái lực với liên kết Actin có thể làm thay đổi quá trình trùng hợp Actin và do đó ảnh hưởng đến kiến trúc tế bào tế bào podocytes. [7]
FSGS2: TRPC6
603965
Một gen thứ hai liên quan đến FSGS là TRPC6, mã hóa một thành viên của họ kênh TRP chính tắc. Họ kênh ion này thực hiện các cation theo cách thức không chọn lọc. Như với ACTN4, TRPC6 được thể hiện trong các tế bào. Trong khi các kênh TRP có thể được kích hoạt thông qua nhiều phương pháp khác nhau, TRPC6 được biết là được kích hoạt bằng kích thích phospholipase C. Có ít nhất 6 đột biến trong kênh này, nằm trên toàn bộ kênh. Ít nhất một trong những đột biến này, P112Q, dẫn đến tăng canxi nội bào. Không rõ làm thế nào điều này có thể dẫn đến FSGS, mặc dù người ta đã đề xuất rằng nó có thể dẫn đến sự thay đổi của động lực học tế bào hoặc giảm bạch cầu. [7]
FSGS3: CD2AP
607832
Một gen khác có thể liên quan đến các dạng FSGS di truyền là gen được gọi là CD2AP (protein liên kết CD2) hoặc CMS (protein liên kết Cas với nhiều miền SH3). Protein được biểu hiện bởi gen này được thể hiện trong các tế bào podocytes nơi nó tương tác với fyn và synolineodin. Có một báo cáo rằng một đột biến ghép nối trong gen này đã được tìm thấy ở hai bệnh nhân có FSGS liên quan đến HIV và điều này dẫn đến sự dịch mã protein bị thay đổi. Điều này đã được lý thuyết hóa dẫn đến thay đổi liên kết actin và do đó, thay đổi cấu trúc tế bào tế bào tế bào. [7]
FSGS4: APOL1
612551
Ở những người gốc Phi, hai biến thể phổ biến trong APOL1 đã được liên kết với FSGS. Người ta tin rằng các biến thể này phát sinh như một cơ chế phòng thủ chống lại Trypanosoma brucei rhodesiense hoặc một số ký sinh trùng cận Sahara khác mặc dù có tính mẫn cảm cao với FSGS khi được di truyền từ cả hai cha mẹ. [8]
FSGS5: INF2
613237
Một gen khác liên quan đến FSGS là INF2, mã hóa một thành viên của họ protein điều hòa Actin. Quan sát cho thấy sự thay đổi trong formin biểu hiện podocyte này gây ra FSGS nhấn mạnh tầm quan trọng của việc điều hòa tốt quá trình trùng hợp Actin trong chức năng của podocyte. [9]
SRN1: NPHS2
600995
Đột biến trong gen NPHS2, mã hóa cho protein được gọi là podocin, [10] có thể gây ra bệnh viêm cầu thận phân đoạn khu trú. [11] Đây là một dạng đột biến của FSGS. [12] Một cá thể bị ảnh hưởng có thể bị đột biến. gen, trái ngược với các dạng bệnh qua trung gian ACTN4 và TRPC6, chiếm ưu thế và chỉ cần một bản sao đột biến của gen. FSGS qua trung gian NPHS2 có khả năng kháng điều trị bằng steroid.
Một số nhà nghiên cứu đã tìm thấy SuPAR là một nguyên nhân của FSGS. [ cần trích dẫn ]
Một gen khác có liên quan đến hội chứng này là gen COL4A5. [13]
[ chỉnh sửa ]
Triệu chứng và dấu hiệu [ chỉnh sửa ]
Ở trẻ em và một số người lớn, FSGS biểu hiện như một hội chứng thận hư, đặc trưng bởi phù nề (liên quan đến phù nề tăng cân), hạ glucose máu (albumin huyết thanh thấp, protein trong máu), tăng lipid máu và tăng huyết áp (huyết áp cao). Ở người lớn, nó cũng có thể xuất hiện dưới dạng suy thận và protein niệu, không có hội chứng thận hư toàn thân.
Các xét nghiệm [ chỉnh sửa ]
Chẩn đoán phân biệt [ chỉnh sửa ]
Điều trị [ 19659075] Phần này trống. Bạn có thể giúp đỡ bằng cách thêm vào nó. ( Tháng 1 năm 2019 )
Từ nguyên [ chỉnh sửa ] Các thành phần riêng lẻ của tên gọi đề cập đến sự xuất hiện của mô thận trên sinh thiết: đầu mối Một số trong số các cầu thận có liên quan (trái ngược với khuếch tán), phân đoạn mỗi cầu thận có liên quan (trái ngược với toàn cầu), [14] xơ hóa cầu thận đối với sẹo của cầu thận (một phần của nephron (đơn vị chức năng của thận)). Xơ hóa cầu thận thường được chỉ định bằng nhuộm PAS nặng và phát hiện immunoglobulin M (IgM) và C3-convertase (C3) trong phân đoạn xơ cứng. [15]
Bệnh nhân đáng chú ý [ chỉnh sửa cũng [ chỉnh sửa ]
Tài liệu tham khảo [ chỉnh sửa ]
- ^ a Kumar V, Fausto N, Abbas A, chủ biên. (2003). Cơ sở bệnh lý của Robbins & Cotran (tái bản lần thứ 7). Saunders. trang 982 từ3. Sê-ri 980-0-7216-0187-8.
- ^ "Xơ hóa cầu thận phân đoạn khu trú" tại Từ điển y khoa của Dorland
- ^ "Bệnh lý thận" . Truy xuất 2008-11-25 .
- ^ Thomas DB, Franceschini N, Hogan SL, et al. (2006). "Đặc điểm lâm sàng và bệnh lý của các biến thể bệnh lý cầu thận phân đoạn khu trú". Thận Int . 69 (5): 920 Chiếc6. doi: 10.1038 / sj.ki.5000160. PMID 16518352.
- ^ Burtis, C.A.; Ashwood, E.R. và Bruns, D.E. Sách giáo khoa Tietz về hóa học lâm sàng và chẩn đoán phân tử. Phiên bản thứ 5. Yêu tinh khác. Trang 1566
- ^ Harrison
- ^ a b c [1965989] TV, Winn MP (2007). "TRPC6 và FSGS: Bệnh lý kênh TRP mới nhất". Biochimica et Biophysica Acta (BBA) – Cơ sở phân tử của bệnh . 1772 (8): 859 Ảo68. doi: 10.1016 / j.bbadis.2007.03.005. PMID 17459670.
- ^ Genovese G, Friedman DJ, Ross MD, Lecordier L, Uzureau P, Freedman BI, Bowden DW, Langefeld CD, Oleksyk TK, Uscinski Knob AL, Berc Nelson GW, Vanhollebeke B, Winkler CA, Kopp JB, Trả tiền E, Pollak MR (tháng 7 năm 2010). "Hiệp hội các biến thể AppanLytic ApoL1 với bệnh thận ở người Mỹ gốc Phi". Khoa học . 329 (5993): 841 Cách5. doi: 10.1126 / khoa học.1193032. PMC 2980843 . PMID 20647424.
- ^ Brown EJ, Schlöndorff JS, Becker DJ, Tsukaguchi H, Uscinski AL, Higgs HN, Henderson JM, Pollak MR (tháng 1 năm 2010). "Đột biến trong protein form2 INF2 gây ra bệnh xơ cứng cầu thận phân đoạn khu trú". Di truyền tự nhiên . 42 (1): 72 Chiếc6. doi: 10.1038 / ng.505. PMC 2980844 . PMID 20023659.
- ^ Tsukaguchi H, Sudhakar A, Le TC, et al. (Tháng 12/2002). "Đột biến NPHS2 trong bệnh xơ cứng cầu thận phân đoạn khởi phát muộn: R229Q là một alen liên quan đến bệnh phổ biến". J. Lâm sàng. Đầu tư . 110 (11): 1659 Ảo66. doi: 10.1172 / JCI16242. PMC 151634 . PMID 12464671.
- ^ Franceschini N, Bắc KE, Kopp JB, McKenzie L, Winkler C (tháng 2 năm 2006). "Gen NPHS2, hội chứng thận hư và xơ hóa cầu thận phân đoạn khu trú: đánh giá HuGE". Genet. Med . 8 (2): 63 Kiếm75. doi: 10.1097 / 01.gim.0000200947.09626.1c. PMID 16481888.
- ^ Boute N, Gribouval O, Roselli S, Benessy F, Lee H, Fuchshuber A, Dahan K, Gubler MC, Niaudet P, Antignac C (tháng 5 năm 2000). "NPHS2, mã hóa protein podocin cầu thận, bị đột biến trong hội chứng thận hư kháng steroid tự phát". Di truyền tự nhiên . 24 (4): 349 Tiết354. đổi: 10.1038 / 74166. PMID 10742096.
- ^ Zhang J, Yang J, Hu Z (2017) Nghiên cứu về một gia đình bị ảnh hưởng với bệnh cầu thận phân đoạn khu trú do đột biến gen COL4A5. Zhonghua Yi Xue Yi Chuan Xue Za Zhi 34 (3): 373-376 doi: 10.3760 / cma.j.issn.1003-9406.2017.03.013
- ^ "Focal_seibutional_glomerulter". Lưu trữ từ bản gốc vào ngày 2009-01 / 07 . Truy xuất 2008-11-25 .
- ^ "Focal_seributional_glomerullyclerosis của thận" . Truy xuất 2009-11-20 .
- ^ http: //www.mlssoney.com/news/article/2014/02/13/kidney-disease-forces-former-new- england-Revolution-dc-united-midfielder-cly
- ^ https://www.irishtimes.com/sport/soney/english-soney/andy-cole-reveals-he-s-been-suffering- từ-thận-suy-1.2417229
- ^ Clarey, Christopher (28 tháng 8 năm 2015). "Ngày trước khi ghép thận, Aries Merritt giành được đồng trong những rào cản". Thời báo New York . Truy xuất 17 tháng 5 2016 .
- ^ "Khám nghiệm tử thi: Những giờ cuối cùng của Natalie Cole." Khám nghiệm tử thi . Nar. Eric Meyers. Thực thi Sản phẩm Ed Taylor và Michael Kelpie. Reelz, ngày 27 tháng 5 năm 2017. Truyền hình.
Đọc thêm [ chỉnh sửa ]
- Wei C, El Hindi S, Li J, Fornoni A, Goes N, Sageshima J, Maiguel D, Karumanchi SA, Yap HK, Saleem M, Zhang Q, Nikolic B, Chaudhuri A, Daftarian P, Salido E, Torres A, Salifu M, Sarwal MM, Schaefer F, Morath C, Schwenger V, Zeier M, Gupta V, Roth D, MP Rastaldi, Burke G, Ruiz P, Reiser J (tháng 7 năm 2011). "Thụ thể urokinase lưu hành như là một nguyên nhân của bệnh cầu thận phân đoạn khu trú". Nat Med . 17 (8): 952 Ảo960. doi: 10.1038 / nm.2411. PMC 4089394 . PMID 21804539.
- Tổ chức NephCure Chỉ cam kết hỗ trợ nghiên cứu tìm kiếm nguyên nhân của Hội chứng thận hư và FSGS, cải thiện việc điều trị và tìm ra phương pháp chữa trị. với các bệnh thận ở trẻ em (FSGS, Hội chứng thận hư và các bệnh khác)
- Nghiên cứu về FSGS Một nhóm các bác sĩ và nhà khoa học thận từ Bệnh viện Brigham và Bệnh viện / Trường Y Harvard làm việc để tìm hiểu thêm về nguyên nhân của FSGS và Hội chứng thận hư ở trẻ em và người lớn, với sự nhấn mạnh vào cơ sở di truyền của những căn bệnh này.
- Tổng quan chung về Bệnh lý thận
- Tahzib M, Frank R, Gauthier B, Valderrama E, Trachtman H (tháng 10 năm 1999). "Điều trị vitamin E của bệnh cầu thận phân đoạn khu trú: kết quả của một nghiên cứu nhãn mở". Nhi khoa. Nephrol . 13 (8): 649 Tiết52. doi: 10.1007 / s004670050674. PMID 10502120. Được lưu trữ từ bản gốc vào ngày 2000-10-11.
- Trình chiếu các vai trò có thể có của SV40 trong bệnh thận Phát hiện SV40 ở bệnh nhân mắc bệnh thận do Jeffrey Kopp, MD Bệnh thận Mục NIDDK, NIH.
Liên kết ngoài [ chỉnh sửa ]
- ^ a Kumar V, Fausto N, Abbas A, chủ biên. (2003). Cơ sở bệnh lý của Robbins & Cotran (tái bản lần thứ 7). Saunders. trang 982 từ3. Sê-ri 980-0-7216-0187-8.
- ^ "Xơ hóa cầu thận phân đoạn khu trú" tại Từ điển y khoa của Dorland
- ^ "Bệnh lý thận" . Truy xuất 2008-11-25 .
- ^ Thomas DB, Franceschini N, Hogan SL, et al. (2006). "Đặc điểm lâm sàng và bệnh lý của các biến thể bệnh lý cầu thận phân đoạn khu trú". Thận Int . 69 (5): 920 Chiếc6. doi: 10.1038 / sj.ki.5000160. PMID 16518352.
- ^ Burtis, C.A.; Ashwood, E.R. và Bruns, D.E. Sách giáo khoa Tietz về hóa học lâm sàng và chẩn đoán phân tử. Phiên bản thứ 5. Yêu tinh khác. Trang 1566
- ^ Harrison
- ^ a b c [1965989] TV, Winn MP (2007). "TRPC6 và FSGS: Bệnh lý kênh TRP mới nhất". Biochimica et Biophysica Acta (BBA) – Cơ sở phân tử của bệnh . 1772 (8): 859 Ảo68. doi: 10.1016 / j.bbadis.2007.03.005. PMID 17459670.
- ^ Genovese G, Friedman DJ, Ross MD, Lecordier L, Uzureau P, Freedman BI, Bowden DW, Langefeld CD, Oleksyk TK, Uscinski Knob AL, Berc Nelson GW, Vanhollebeke B, Winkler CA, Kopp JB, Trả tiền E, Pollak MR (tháng 7 năm 2010). "Hiệp hội các biến thể AppanLytic ApoL1 với bệnh thận ở người Mỹ gốc Phi". Khoa học . 329 (5993): 841 Cách5. doi: 10.1126 / khoa học.1193032. PMC 2980843 . PMID 20647424.
- ^ Brown EJ, Schlöndorff JS, Becker DJ, Tsukaguchi H, Uscinski AL, Higgs HN, Henderson JM, Pollak MR (tháng 1 năm 2010). "Đột biến trong protein form2 INF2 gây ra bệnh xơ cứng cầu thận phân đoạn khu trú". Di truyền tự nhiên . 42 (1): 72 Chiếc6. doi: 10.1038 / ng.505. PMC 2980844 . PMID 20023659.
- ^ Tsukaguchi H, Sudhakar A, Le TC, et al. (Tháng 12/2002). "Đột biến NPHS2 trong bệnh xơ cứng cầu thận phân đoạn khởi phát muộn: R229Q là một alen liên quan đến bệnh phổ biến". J. Lâm sàng. Đầu tư . 110 (11): 1659 Ảo66. doi: 10.1172 / JCI16242. PMC 151634 . PMID 12464671.
- ^ Franceschini N, Bắc KE, Kopp JB, McKenzie L, Winkler C (tháng 2 năm 2006). "Gen NPHS2, hội chứng thận hư và xơ hóa cầu thận phân đoạn khu trú: đánh giá HuGE". Genet. Med . 8 (2): 63 Kiếm75. doi: 10.1097 / 01.gim.0000200947.09626.1c. PMID 16481888.
- ^ Boute N, Gribouval O, Roselli S, Benessy F, Lee H, Fuchshuber A, Dahan K, Gubler MC, Niaudet P, Antignac C (tháng 5 năm 2000). "NPHS2, mã hóa protein podocin cầu thận, bị đột biến trong hội chứng thận hư kháng steroid tự phát". Di truyền tự nhiên . 24 (4): 349 Tiết354. đổi: 10.1038 / 74166. PMID 10742096.
- ^ Zhang J, Yang J, Hu Z (2017) Nghiên cứu về một gia đình bị ảnh hưởng với bệnh cầu thận phân đoạn khu trú do đột biến gen COL4A5. Zhonghua Yi Xue Yi Chuan Xue Za Zhi 34 (3): 373-376 doi: 10.3760 / cma.j.issn.1003-9406.2017.03.013
- ^ "Focal_seibutional_glomerulter". Lưu trữ từ bản gốc vào ngày 2009-01 / 07 . Truy xuất 2008-11-25 .
- ^ "Focal_seributional_glomerullyclerosis của thận" . Truy xuất 2009-11-20 .
- ^ http: //www.mlssoney.com/news/article/2014/02/13/kidney-disease-forces-former-new- england-Revolution-dc-united-midfielder-cly
- ^ https://www.irishtimes.com/sport/soney/english-soney/andy-cole-reveals-he-s-been-suffering- từ-thận-suy-1.2417229
- ^ Clarey, Christopher (28 tháng 8 năm 2015). "Ngày trước khi ghép thận, Aries Merritt giành được đồng trong những rào cản". Thời báo New York . Truy xuất 17 tháng 5 2016 .
- ^ "Khám nghiệm tử thi: Những giờ cuối cùng của Natalie Cole." Khám nghiệm tử thi . Nar. Eric Meyers. Thực thi Sản phẩm Ed Taylor và Michael Kelpie. Reelz, ngày 27 tháng 5 năm 2017. Truyền hình.