|
|||
 |
|||
| Tên | |||
|---|---|---|---|
| Tên IUPAC ưa thích | |||
| Tên IUPAC có hệ thống | |||
| Tên khác
Ôxít Osmium (VIII) |
|||
| ChEBI | |||
| ChemSpider | |||
| Thẻ thông tin ECHA | 100.040.038 | ||
| Số EC | 244-058-7 | ||
| MeSH | Osmium + tetroxide | ||
| Số RTECS | RN1140000 | ||
| Số UN | UN 2471 | ||
| |||
| OsO 4 | |||
| Khối lượng mol | 254,23 g / mol | ||
| Xuất hiện | chất rắn dễ bay hơi màu trắng | ||
| Mùi | vị chát, giống như clo | ||
| Mật độ | 4,9 g / cm 3 [1] | ||
| Điểm nóng chảy | 40,25 ° C (104,45 ° F; 313,40 K) | ||
| Điểm sôi | 129,7 ° C (265,5 ° F; 402,8 K) | ||
| 5,70 g / 100 mL (10 ° C) 6,23 g / 100 mL (25 ° C) |
|||
| Độ hòa tan | 375 g / 100 mL (CCl 4 ) hòa tan trong hầu hết các dung môi hữu cơ, amoni hydroxit, phốt pho oxychloride |
||
| Áp suất hơi | 7 mmHg (20 ° C) [2] | ||
| Cấu trúc | |||
| Monoclinic, mS20 | |||
| C2 / c; a = 0,4515 nm, b = 0,52046 nm, c = 0,80938 nm, α = 77,677 °, β = 73,784 °, γ = 64.294 ° [3] | |||
| Nguy cơ | |||
| Bảng dữ liệu an toàn | ICSC 0528 | ||
| |
|||
| Cụm từ R (lỗi thời) | R26 / 27/28 R34 | ||
| Cụm từ S (lỗi thời) | (S1 / 2) S7 / 9 S26 , S45 | ||
| NFPA 704 |
|
||
| Liều lượng hoặc nồng độ ( LD LC ): | |||
| 1316 mg / m 3 (thỏ, 30 phút) 423 mg / m 3 (chuột, 4 giờ) 423 mg / m 3 (chuột, 4 giờ) [4] |
|||
| Giới hạn phơi nhiễm sức khỏe của Hoa Kỳ (NIOSH): | |||
| TWA 0,002 mg / m 3 [2] | |||
| TWA 0,002 mg / m 3 (0,0002 ppm) ST 0,006 mg / m 3 (0,0006 ppm) [2] [19459] | |||
| 1 mg / m 3 [2] | |||
| Các hợp chất liên quan | |||
| Ruthenium tetroxide | |||
| Ôxít Osmium (IV) | |||
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu ở trạng thái tiêu chuẩn của chúng (ở 25 ° C [77 °F]100 kPa).
|
|||
| Tham chiếu hộp thông tin | |||
Osmium tetroxide (cũng osmium (VIII) oxit ) là hợp chất hóa học có công thức OsO 4 . Hợp chất này đáng chú ý vì nhiều công dụng của nó, mặc dù độc tính và hiếm của osmium. Nó cũng có một số tính chất thú vị, một là chất rắn dễ bay hơi. Hợp chất này không màu, nhưng hầu hết các mẫu đều có màu vàng. [5] Điều này rất có thể là do sự có mặt của tạp chất OsO 2 có màu vàng nâu. [6]
Tính chất vật lý [ chỉnh sửa ]
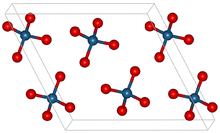
Ôxít Osmium (VIII) tạo thành tinh thể monoclinic. [3][7] Nó có mùi giống như mùi clo đặc trưng. Tên nguyên tố osmium có nguồn gốc từ osme tiếng Hy Lạp cho mùi . OsO 4 rất dễ bay hơi: nó thăng hoa ở nhiệt độ phòng. Nó hòa tan trong một loạt các dung môi hữu cơ. Nó cũng hòa tan vừa phải trong nước, mà nó phản ứng thuận nghịch để tạo thành axit osmic (xem bên dưới). [8] Oxit tinh khiết osmium (VIII) có lẽ không màu [9] và người ta cho rằng màu vàng của nó là do tạp chất osmium dioxide (OsO 2 ). [10] Phân tử osmium tetroxide là tứ diện và do đó không phân cực. Tính không phân cực này giúp OsO 4 thâm nhập vào màng tế bào tích điện. OsO 4 hòa tan trong carbon tetrachloride gấp 518 lần so với trong nước.
Cấu trúc và cấu hình electron [ chỉnh sửa ]
osmium của OsO 4 có số oxi hóa là VIII; tuy nhiên, kim loại không có điện tích 8+ tương ứng vì liên kết trong hợp chất phần lớn là hóa trị (năng lượng ion hóa cần thiết để tạo ra điện tích 8+ chính thức cũng vượt xa năng lượng có sẵn trong các phản ứng hóa học thông thường). Nguyên tử osmium có tám electron hóa trị (6s 2 5d 6 ) với liên kết đôi với bốn phối tử oxit dẫn đến phức hợp 16 electron. Đây là đẳng lượng với các ion permanganat và cromat.
Tổng hợp [ chỉnh sửa ]
OsO 4 được hình thành chậm khi bột osmium phản ứng với O 2 ở nhiệt độ môi trường. Phản ứng của chất rắn khối lượng lớn đòi hỏi phải làm nóng đến 400 ° C. [11]
- Phản ứng [ chỉnh sửa ]
Oxy hóa anken [ chỉnh sửa ]
] 4 để cung cấp cho các loài diolate thủy phân thành cis -diols. Quá trình ròng được gọi là dihydroxylation. Quá trình này diễn ra thông qua phản ứng tuần hoàn [3 + 2] giữa OsO 4 và anken để tạo thành este osmate trung gian nhanh chóng thủy phân để tạo ra diol phụ. Khi các nguyên tử oxy được thêm vào trong một bước phối hợp, hóa học lập thể thu được là cis .
-
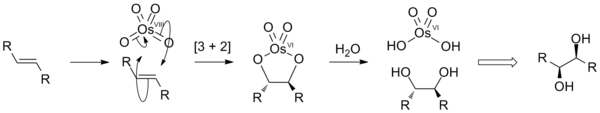 Việc mô tả lý tưởng hóa quá trình khử cis-dihydroxyl hóa anken.
Việc mô tả lý tưởng hóa quá trình khử cis-dihydroxyl hóa anken.
OsO 4 rất tốn kém và có độc tính cao, khiến nó trở thành thuốc thử không hấp dẫn khi sử dụng với lượng hóa trị. Tuy nhiên, các phản ứng của nó được thực hiện xúc tác bằng cách thêm chất tái oxy hóa để tái oxy hóa sản phẩm phụ Os (VI) trở lại Os (VIII). Các thuốc thử điển hình bao gồm H 2 O 2 (Milas hydroxylation), N-methylmorpholine N-oxide (Upjohn dihydroxylation) và K 3 Fe (1945) 6 / nước. Các chất tái oxy hóa này không tự phản ứng với các anken. Các hợp chất osmium khác có thể được sử dụng làm chất xúc tác, bao gồm muối osmate (VI) ([OsO 2 (OH) 4 )] 2− và osmium trichloride (OsCl 3 · x H 2 O). Những loài này oxy hóa thành osmium (VIII) với sự có mặt của các chất oxy hóa như vậy. [12]
Các bazơ Lewis như amin bậc ba và pyridin làm tăng tốc độ khử nước. "Gia tốc phối tử" này phát sinh thông qua sự hình thành chất bổ sung OsO 4 L, chất này nhanh chóng bổ sung vào anken. Nếu amin là chirus, thì quá trình dihydroxyl hóa có thể tiến hành với enantioselectivity (xem Sharhydroxylation không đối xứng). [13] OsO 4 không phản ứng với hầu hết các carbohydrate. [1945] Quá trình này có thể được mở rộng để cung cấp cho aldehyd trong quá trình oxy hóa Lemieux, Johnson, sử dụng định kỳ để đạt được sự phân tách diol và tái tạo tải lượng xúc tác của OsO 4 . Quá trình này tương đương với quá trình ozon hóa.
Hóa học phối hợp [ chỉnh sửa ]
OsO 4 là một axit Lewis và là chất oxy hóa nhẹ. Nó phản ứng với dung dịch nước kiềm để tạo ra anion perosmate OsO
4 (OH) 2−
2 . [15] osmate anion, OsO
2 (OH) 4−
4 .Khi căn cứ Lewis là một amin, các chất gây nghiện cũng được hình thành. Do đó, OsO 4 có thể được lưu trữ dưới dạng osmeth trong đó OsO 4 được tạo phức với hexamine. Osmeth có thể được hòa tan trong tetrahydrofuran (THF) và pha loãng trong dung dịch đệm dung dịch nước để tạo ra dung dịch làm việc pha loãng (0,25%) của OsO 4 . [16]
-BuNH 2 đạo hàm imido được sản xuất:
- OsO 4 + Tôi 3 CNH 2 → OsO 3 (NCMe 3 2 O
Tương tự, với NH 3 người ta thu được phức nitrido:
- OsO 4 + NH 3 + KOH → K [Os(N)O 3 ] + 2 H 2 O [19659145] [Os(N)O 3 ] – anion là đẳng điện và đẳng cấu với OsO 4 .
OsO 4 rất hòa tan trong rượu tert-butyl. Trong dung dịch, nó dễ dàng bị khử bởi hydro thành kim loại osmium. Kim loại osmium lơ lửng có thể được sử dụng để xúc tác hydro hóa một loạt các hóa chất hữu cơ có chứa liên kết đôi hoặc ba.
- OsO 4 + 4 H 2 → Os + 4 H 2 O
OsO 4 trải qua quá trình "khử cacbon" với carbon monoxide trong metanol ở 400 K và 200 sbar để tạo ra cụm tam giác Os 3 (CO) 12 :
- 3 OsO 4 + 24 CO → Os 3 (CO) 12 + 12 CO 2 [11]
Oxofluorides chỉnh sửa ]
Osmium tạo thành một số oxofluoride, tất cả đều rất nhạy cảm với độ ẩm. Màu tím cis -OsO 2 F 4 hình thành ở 77 K trong dung dịch HF khan: [17] ] 4 + 2 KrF 2 → cis -OsO 2 F 4 + 2 Kr + O 2
OsO 4 cũng phản ứng với F 2 để tạo thành OsO màu vàng 3 F 2 :
- 2 OsO 4 + 2 F 2 → 2 OsO 3 F 2 + O 2
OsO 4 phản ứng với một tương đương với [Me 4 N] F ở 298 K và 2 tương đương tại 253 K: [11] 19659144] OsO 4 + [Me 4 N] F → [Me 4 N] [OsO 4 F]
-
- 4 + 2 [Tôi 4 N] F → [Tôi 4 N] 2 [ cis -OsO 4 F 2 ]
Tổng hợp hữu cơ ]
Trong tổng hợp hữu cơ OsO 4 được sử dụng rộng rãi để oxy hóa anken thành các diol phụ, thêm hai nhóm hydroxyl ở cùng một phía (bổ sung đồng bộ). Xem phản ứng và cơ chế trên. Phản ứng này đã được thực hiện cả xúc tác (Upjohn dihydroxylation) và không đối xứng (dihydroxylation không đối xứng).
Ôxít Osmium (VIII) cũng được sử dụng với số lượng xúc tác trong quá trình oxy hóa Shar Xếp để tạo ra các amino-alcol độc.
Kết hợp với định kỳ natri, OsO 4 được sử dụng để phân tách oxy hóa alkenes (oxy hóa Lemieux-Johnson) khi định kỳ phục vụ cả hai để tách diol được tạo thành bởi dihydroxyl hóa và khử oxy hóa 3 trở lại OsO 4 . Sự biến đổi ròng giống hệt với sự biến đổi được tạo ra bởi quá trình ozon hóa. Dưới đây là một ví dụ từ tổng hợp Isosteviol. [19]
Nhuộm sinh học [ chỉnh sửa ]
OsO 4 là chất nhuộm màu được sử dụng rộng rãi được sử dụng trong kính hiển vi điện tử truyền qua (TEM) để cung cấp độ tương phản với hình ảnh. 19659170] Là một vết lipid, nó cũng hữu ích trong việc soi kính hiển vi điện tử (SEM) như là một thay thế cho lớp phủ phún xạ. Nó nhúng một kim loại nặng trực tiếp vào màng tế bào, tạo ra tốc độ tán xạ electron cao mà không cần phải phủ màng bằng một lớp kim loại, có thể che khuất các chi tiết của màng tế bào. Trong nhuộm màu của màng plasma, osmium (VIII) liên kết với các vùng đầu phospholipid, do đó tạo ra sự tương phản với các nguyên sinh chất lân cận (tế bào chất). Ngoài ra, oxit osmium (VIII) cũng được sử dụng để cố định các mẫu sinh học kết hợp với HgCl 2 . Khả năng tiêu diệt nhanh của nó được sử dụng để nhanh chóng tiêu diệt các mẫu vật sống như động vật nguyên sinh. OsO 4 ổn định nhiều protein bằng cách biến đổi chúng thành gel mà không phá hủy các đặc điểm cấu trúc. Các protein mô được ổn định bởi OsO 4 không bị đông tụ bởi rượu trong quá trình khử nước. [14] Ôxít Osmium (VIII) cũng được sử dụng làm chất nhuộm cho lipit trong kính hiển vi quang học. [21] cũng nhuộm giác mạc của con người (xem các cân nhắc về an toàn).

Nhuộm polymer [ chỉnh sửa ]
Nó cũng được sử dụng để nhuộm copolyme, ví dụ được biết đến nhiều nhất là copolyme. trong đó một pha có thể được nhuộm màu để hiển thị cấu trúc vi mô của vật liệu. Ví dụ, copolyme khối styrene-butadien có chuỗi polybutadiene trung tâm với mũ kết thúc bằng polystyrene. Khi được xử lý bằng OsO 4 ma trận butadien phản ứng tốt hơn và do đó hấp thụ oxit. Sự hiện diện của một kim loại nặng là đủ để chặn chùm electron, vì vậy các miền polystyrene được nhìn thấy rõ ràng trong các màng mỏng trong TEM.
Tinh chế quặng Osmium [ chỉnh sửa ]
OsO 4 là chất trung gian trong việc chiết xuất osmium từ quặng của nó. Dư lượng có chứa Osmium được xử lý bằng natri peroxide (Na 2 O 2 ) tạo thành Na 2 [OsO 4 (OH) ] 2 ]hòa tan. Khi tiếp xúc với clo, muối này mang lại cho OsO 4 . Trong giai đoạn tinh chế cuối cùng, OsO thô 4 được hòa tan trong rượu NaOH tạo thành Na 2 [OsO 2 (OH) 4 , mà, khi được điều trị bằng NH 4 Cl, để cho (NH 4 ) 4 [OsO 2 Cl 2 ]. Muối này được khử dưới hydro để cung cấp osmium. [8]
Chất bổ sung Buckminsterfullerene [ chỉnh sửa ]
OsO 4 được phép xác nhận mô hình bóng đá của bóng đá. một nguyên tử cacbon 60 nguyên tử. Phần bổ sung, được hình thành từ một dẫn xuất của OsO 4 là C 60 (OsO 4 ) (4- tert -butylpyridine 2 . Chất bổ sung đã phá vỡ tính đối xứng của fullerene, cho phép kết tinh và xác nhận cấu trúc của C 60 bằng phương pháp tinh thể học tia X. [22]
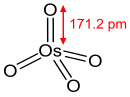


![{ displaystyle { ce {Os + 2O2 -> [Delta T] OsO4}}} "/> </span></dd>
</dl>
<h2><span class=](https://wikimedia.org/api/rest_v1/media/math/render/svg/8d2c2ac06e64cd164869ed5506f13c3cfa320d70) Phản ứng
Phản ứng 